Kasuistik
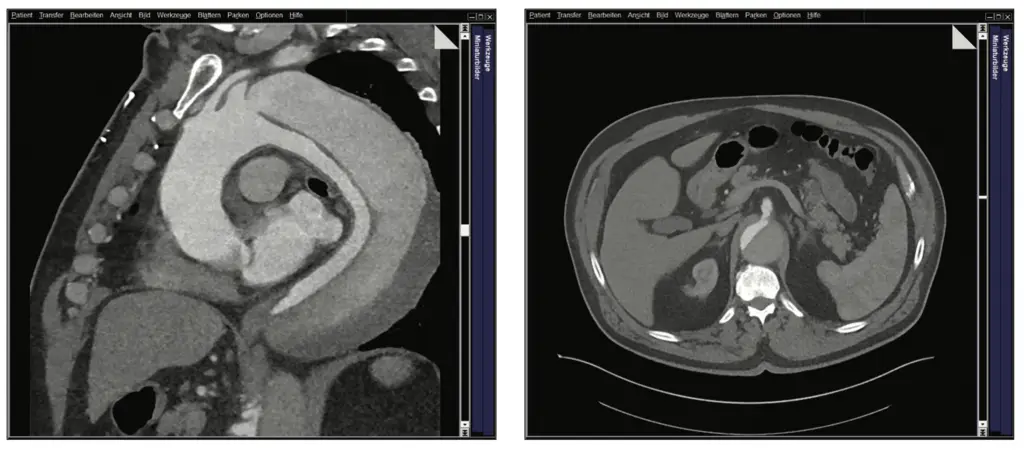
Im Herbst 2023 wurde bei dem damals 62-jährigen Mann als Zufallsbefund im Rahmen einer urologisch veranlassten CT-Untersuchung eine komplexe thorakoabdominelle Aortendissektion Typ Standford B diagnostiziert. Distal setzte sich die Dissektion in ein mutmaßlich vorbestehendes infrarenales Aortenaneurysma fort und bildete ein Aneurysma dissecans von 8 cm Durchmesser. Die Dissektion endete in der linken A. iliaca externa. Zudem bestanden Aneurysmata der A. iliaca externa. Das wahre Lumen war schmächtig im Sinne eines subtotalen True-Lumen-Kollaps.
Klinisch bestanden ätiologisch nicht sicher einzuordnende Rückenschmerzen, die spontan sistierten. Es bestanden keine Zeichen einer Ischämie.
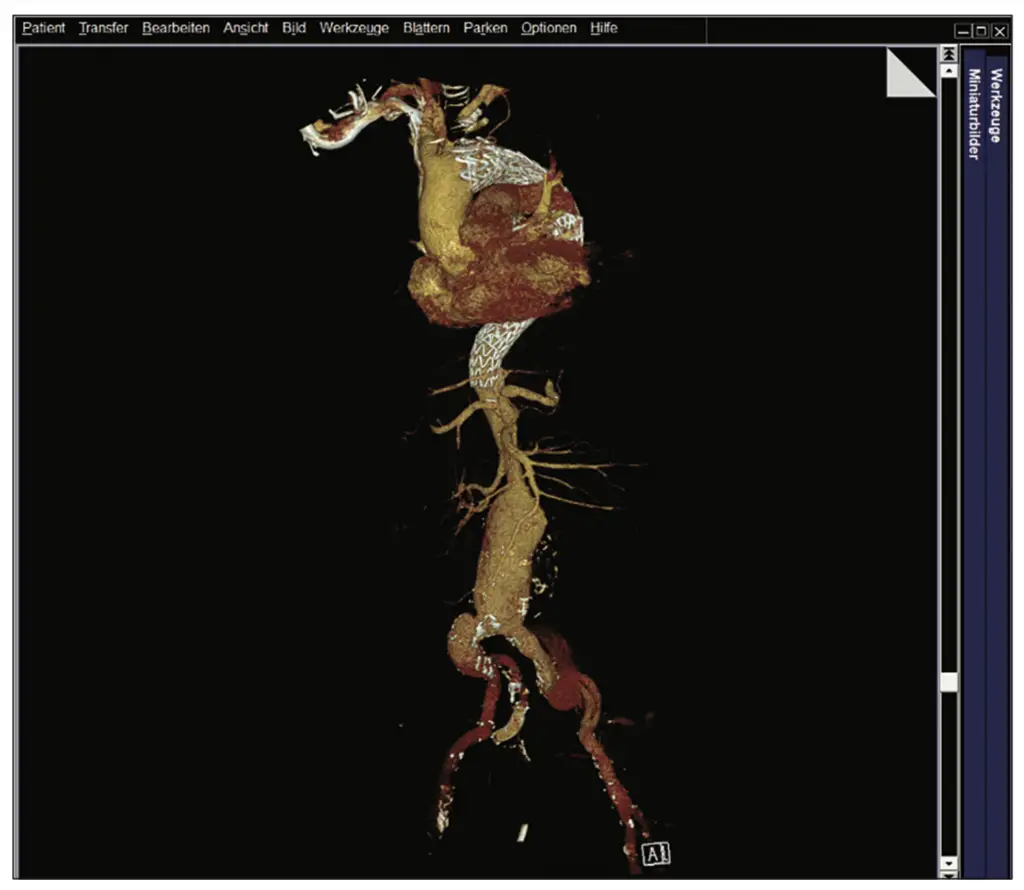
In interdisziplinären Fallkonferenzen wurden die möglichen Versorgungsoptionen diskutiert und schließlich fiel unter Einbeziehung des Patienten die Entscheidung zu einer dreizeitigen endovaskulären Versorgung. Zunächst erfolgte eine Versorgung der thorakalen Aorta mittels Stentgrafts, die proximale Landezone musste dabei nach vorherigem Debranching mittels Carotido-Carotido-Subclavia-Bypass bis in die Zone 1 nach Ishimaru ausgeweitet werden. Distal erfolgte eine Versorgung der Dissektion der Beckenarterien mit Ausschaltung der Iliacalaneurysmata durch eine beidseitige Implantation eines Iliac-Side-Branch-Devices (Abb. 1 a–c).
Im Dezember 2023 war die abschließende Versorgung mittels individuell angefertigtem thorakoabdominellen Multibranch-Aortenstent mit Landezone in den zuvor implantierten Stents suprarenal bzw. iliacal beidseits geplant. Anatomisch waren zu diesem Zeitpunkt verschiedene Aspekte bekannt und wurden in die OP-Planung, auch zeitlich, miteingeschlossen.
Aufgrund des schmächtigen wahren Lumens sollten Truncus coeliacus, A. mesenterica superior und rechte Nierenarterie mittels Inner-Branches (Custom Design der Firma Jotec/Artivion) erhalten werden. Die linke Nierenarterie wurde explizit nicht miteingeschlossen, da von einem initial funktionslosen Organ ausgegangen wurde.
Als anatomische Normvariante zeigte sich in der Bildgebung ein isolierter Abgang der A. hepatica sin. aus der Aorta entspringend. Geplant war, diesen mit einem Twin-Branch (A. hepatica sin./Truncus coeliacus) zu erhalten. Leider kam es nach der Implantation in den Truncus coeliacus zu einer Kompression und damit zu einem Verschluss der A. hepatica sin. Der entsprechende Anteil des Twin-Branches wurde mittels Vascular-Plug verschlossen.
Aufgrund der bereits erfolgten Voroperationen gab es neben der Anatomie weitere Überlegungen, die eine Verlängerung der Operationsdauer erwarten ließen.
Normalerweise werden die Inner-Branches im Aortenstent von kranial über einen links axillären Zugang sondiert, wonach die Stents in die jeweiligen Zielgefäße eingebracht werden. In dem hier beschriebenen Fall war der übliche Zugang von der rechten Axilla aufgrund des vorherigen Debranchings nicht möglich. Auf einen Zugang von der rechten Axilla sollte primär verzichtet werden, da hier ein erhöhtes Apoplex-Risiko bestand. Dieses ergab sich aufgrund der langen Liegedauer der Schleusen im Truncus brachiocephalicus mit allen supraaortalen Ästen. Daher wurde versucht, die Inner-Branches von kaudal durch eine steuerbare Schleuse zu sondieren. Dies war durch den True-Lumen-Kollaps deutlich erschwert. Letztlich gelang auf diesem Wege nur eine Sondierung der A. mesenterica sup., die Sondierung der anderen Gefäße gelang nicht. Aus diesem Grund musste schließlich der vorher abgelehnte Zugang rechts axillär gewählt werden, mit entsprechender Umlagerung des Patienten und Schaffung eines chirurgischen Zugangs.
Da aufgrund der genannten Komplexität von einer verlängerten OP-Dauer mit entsprechender möglicher peripherer Ischämiezeit auszugehen war, wurde sich für eine intraoperative Bypass-Versorgung beider Beine mittels pulsatiler va-ECMO entschieden. Die Hypothese war eine durch die simulierte Pulsatilität reduzierte Extremitäten-Minderperfusion. Zeitgleich sollte die technische und physiologische Machbarkeit eines solchen ECMO-Bypasses gezeigt und die physiologische Flusseigenschaften simuliert werden, um bei größeren und umfangreicheren Eingriffen eine ausreichende pulsatile Organperfusion, beispielsweise über die Nierenarterien, herstellen zu können. In diesem Zuge wurden auch die erheblich höheren Kosten des CARL-Systems gegenüber anderen etablierten Lösungen, wie beispielsweise passiver Schleusenperfusion oder anderen Bypässen, in Kauf genommen. Die Nutzung einer Herz-Lungen-Maschine (HLM) mit Rollerpumpe schied aufgrund der Nichtverfügbarkeit in der Klinik aus.
Ein ECMO-Bypass wird bei solchen Operationen in diversen gefäßchirurgischen und maximalversorgenden Zentren angewendet, da einer der Vorteile die relativ niedrige Heparinisierung unter ECMO gegenüber anderen Verfahren ist und damit eine niedrigere Blutungskomplikation darstellt.
Während der gefäßchirurgischen Aufklärung zu besagtem Eingriff wurde dem Patienten und seinen Angehörigen das Verfahren des extrakorporalen Bypasses dargestellt und auf die erhofften positiven Effekte, wie aber auch auf das erhebliche Komplikationspotenzial hingewiesen. Der Patient willigte in diese OP und das beschriebene Verfahren des ECMO-Bypasses ein.


Verwendet wurde für den ECMO-Bypass eine CARL® (“controlled automated reperfusion of the whole body”) der Firma Resuscitec. Diese ECMO hat in der aktuellen Softwareversion standardmäßig zwei Betriebsmodi, neben dem ECLS-Modus mit Pulsation einen ECMO-Modus, bei dem die zweite Pumpe mit einer Umdrehungsdifferenz von maximal 3000/Minute im laminaren Fluss betrieben werden kann. Im aktuellen Set ist der Oxygenator der Fresenius-Konsole Xenios verbaut. Dieser hat ein Coating, um Thrombenbildung zu verringern, hingegen ist das Schlauchsystem nicht beschichtet. Daher wird das Set regelhaft mit Albumin geprimt. Der Einsatz der CARL für dieses Verfahren war ein Off-Label-Use.
Für den Fluss des Bypasses wurde der pulsatile ECLS-Modus der CARL gewählt.
Folgende va-ECMO-Konfiguration wurde gewählt:
Als Drainage-Kanüle wurde eine 19 Fr.-HLS-Kanüle der Firma Getinge in die V. cava inferior über die rechte V. femoralis eingelegt. Die Rückgabe erfolgte über zwei BioMedicus 10 Fr.-Kanülen der Firma Medtronic jeweils in die A. femoralis superficialis beidseits. Die Schläuche wurden über Adapter von 3/8“ auf 1/4“ reduziert. Gleichzeitig wurden die beiden arteriellen Linien mit Flussminderern bestückt (Abb. 2). Die Implantation der Kanülen und Etablierung des ECMO-Flusses erfolgte vor der eigentlichen OP und vor der Okklusion der Gefäße.
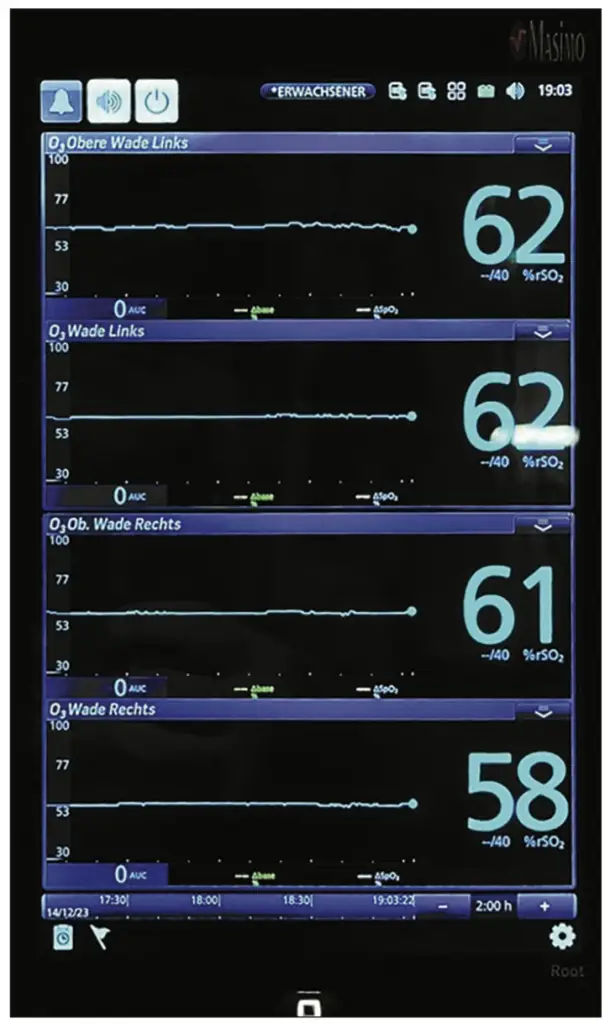
Die Überwachung der Beinperfusion wurde mittels einer NIRS (Nahinfrarot Spektroskopie) der Firma Masimo in der jeweils vorderen und hinteren Muskelloge beider Waden dargestellt. Zusätzlich gab es eine beidseitige Messung der Sauerstoffsättigung (Abb. 3).
Von Beginn der Okklusion an wurden dauerhaft konstante Flüsse der ECMO mit 1,0–1,2 l/min etabliert und über die gesamte Zeitdauer eine Pulsationsfrequenz von 50/min. (Abb. 4).
Da eine Heparinisierung schon aufgrund der Operationsmethode notwendig war, wurden zur Steuerung der Gerinnung regelmäßige pTT-Kontrollen mit einem Zielwert um 60 Se-kunden vorgenommen. Begleitende ACT-Werte waren in dem Aufbau zu ungenau und wichen häufig von den pTT-Werten ab.
Die kumulative OP-Dauer betrug ca. 10 Stunden, davon der ECMO-Bypass ca. 8 Stunden, da durch die Voroperationen und das massiv veränderte Gefäßsystem des Patienten im Verlauf der Operation ein alternativer Zugangsweg geschaffen werden musste.
Nachdem alle Gefäße nach Implantation der Stents und Branches wieder geöffnet waren, wurden der ECMO-Fluss beendet, alle Kanülen entfernt und die Gefäßzugänge chirurgisch verschlossen. Zur postoperativen Überwachung wurde der Patient auf der Intensivstation nachbeatmet, allerdings nach Kontrolle von laborchemischen Parametern, Temperatur, hämodynamischem und respiratorischem System zeitnah ins Weaning genommen und schließlich noch am gleichen Tag extubiert.
Hinsichtlich der primären Hypothese der Vermeidung einer Minderperfusion der Beine zeigten sich alle postoperativen Untersuchungen positiv. Makroskopisch gab es keine Farbveränderungen der Haut und keine Schwellungen oder Ödeme. Auch waren keine Anzeichen hinsichtlich einer Hyperperfusion zu erkennen. Die abgeleiteten peripheren Sauerstoffsättigungen waren unauffällig, ebenso die in festen Intervallen erhobenen Dopplersignale und die laborchemischen Laktat- und CK-Werte.
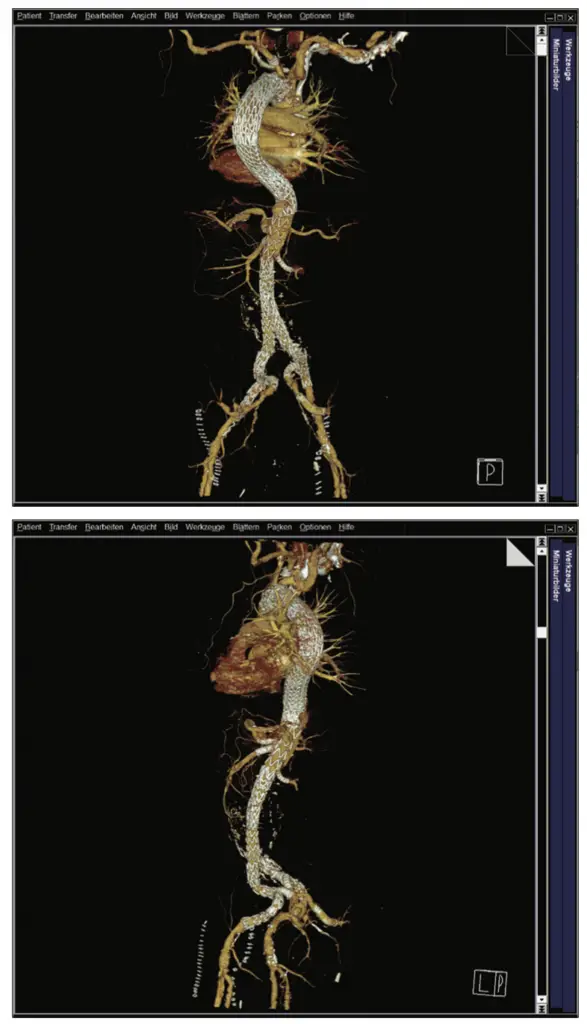
Trotz dieser positiven Befunde wurde ein langer intensivstationärer Aufenthalt notwendig, da es postoperative Komplikationen wie ein akutes Nierenversagen, eine Pneumonie und ein Delir gab. Allerdings entwickelte sich der Gesamtverlauf schließlich positiv und der Patient konnte über die Reha in die Häuslichkeit entlassen werden. Bildgebend waren die Aneurysmata (abgesehen von einem kleinen Typ 2 Endoleak) ausgeschaltet und die Dissektion regelhaft angelegt. Die Stentgrafts waren einschließlich der viszeralen und iliacalen Branches regelhaft perfundiert (Abb. 5 a und b).
In der weiteren Compliance des Patienten zeigte sich nach Entlassung aus der Reha ein lost-to follow-up, die Nachsorge-Kontrollen in der Klinik wurden nicht wahrgenommen, ebenso gelang eine Kontaktaufnahme bisher nicht.
Diskussion
Dass ein pulsatiler Fluss vorteilhaft für die Organperfusion und Mikrozirkulation ist, ist hinreichend bekannt. Schon 1979 konnte tierexperimentell gezeigt werden, dass die Funktionen von Leber und Pankreas nach Etablierung eines laminaren Flusses deutlich abnehmen [1]. Viele Jahre später konnte an aortokoronaren Bypasspatienten gezeigt werden, dass ein pulsatiler Fluss eine bessere Mikrozirkulation zur Folge hat und dies an niedrigeren Laktatwerten als Surrogatparametern festgemacht werden kann [2].
Dies veranlasste das Team zu der Hypothese, dass die Technik des ECMO-Bypasses bei großen gefäßchirurgischen Eingriffen mit langer OP-Dauer durch die Erweiterung mittels eines pulsatilen Flusses positive Auswirkungen auf die Mikrozirkulation haben könnte und damit konsekutiv eine Abnahme von Ischämie-Komplikationen einhergehen könnte. Um eine Machbarkeit mit dem CARL-System zu untersuchen, wurde das System im ersten Schritt allerdings lediglich zur Beinperfusion angewendet, um es später auf die gesamte Organperfusion zu erweitern.
Für die reine Beinperfusion bei Gefäßoperationen stehen heutzutage verschiedene etablierte Konzepte zur Verfügung, etwa pulsatile Systeme unter Verwendung von Schleusen oder axillofemoralen Bypässen, wie sie auch in der Literatur beschrieben sind [3]. Diese Alternativen, ebenfalls funktionierende Systeme, sollten bei der Bewertung pulsatiler Beinperfusion mittels ECMO berücksichtigt werden, aus medizinischer und ökonomischer Sicht.
An der Uniklinik Dresden werden bereits seit 2015 gefäßchirurgische Eingriffe unter va-ECMO-Bypass erfolgreich durchgeführt [4]. Neben verminderten Organischämien ist die relativ niedrige Notwendigkeit für eine Heparinisierung ein großer Vorteil für den Operateur. In Dresden wurde bis dato die Cardiohelp der Firma Getinge verwendet, die lediglich einen laminaren Fluss herstellt und nicht wie in unserem CaseReport eine CARL mit pulsatilem Fluss.
Die Technik wurde in Dresden mit Prof. Reps neu eingeführt, jedoch ist das grundsätzliche Konzept, thorakoabdominelle Aorteneingriffe unter Einsatz eines extrakorporalen Bypasses bzw. ECMO-ähnlicher Verfahren durchzuführen, bereits seit vielen Jahren bekannt; es existieren hierzu größere Serien insbesondere von Coselli aus Houston/Texas, die die Sicherheit und Effektivität solcher extrakorporalen Bypass-Strategien bei komplexen Aorteneingriffen zeigen. Dies ordnet die vorliegende Kasuistik in einen bereits länger bestehenden, international etablierten Kontext ein [5].
Im Vergleich des extrakorporalen Bypasses mittels ECMO mit alternativen Perfusionsverfahren zur Beinperfusion (z. B. axillofemoraler Bypass, distale Perfusionskanüle, Shunt Systeme über Schleusen) zeigt sich, dass ECMO-basierte Systeme den Vorteil einer sehr gut steuerbaren, potenziell pulsatilen Perfusion mit präziser Kontrolle von Fluss, Druck und Gaswechsel bieten, dafür aber technisch komplexer sind und ein höheres Maß an Perfusionserfahrung sowie ein aufwendigeres Monitoring erfordern. Ebenfalls sind die Kosten für Material und Personal wesentlich höher. Alternative Verfahren wie axillofemorale Bypässe oder temporäre Shunts
über Schleusen sind demgegenüber meist schneller und mit weniger apparativem Aufwand zu etablieren. Sie können die Extremitätenischämie effektiv verhindern und kommen ohne vollständiges ECMO-Setup aus, liefern jedoch häufig nur einen weniger gut kontrollierbaren, teilweise nicht-pulsatilen Fluss und sind hinsichtlich Volumensteuerung und Oxygenierung limitiert. Für endovaskuläre Aorteneingriffe mit längerer femoraler Okklusion und hohem Ischämierisiko kann ein pulsatiler ECMO-Bypass wie im beschriebenen Setting daher eine besonders attraktive Option darstellen, solange die höhere Komplexität gerechtfertigt ist; in Situationen mit kürzerer Okklusionsdauer oder limitierten Ressourcen bleiben die etablierten Shunt- und Bypasstechniken sinnvolle und in vielen Zentren gut funktionierende Alternativen.
Aus Daten von akuten Aortendissektionen und kardialen operativen Interventionen weiß man, dass die viszerale Malperfusion nicht trivial ist und mit einer Mortalitätsrate von 50 % eine schwerwiegende Komplikation darstellt. Zwar dreht es sich dabei häufig um Ischämien zu Beginn der Dissektion, es verdeutlicht aber die Brisanz einer Minderperfusion [6].
Wichtige Faktoren sind hierbei der viszerale Perfusionsdruck und die konsekutive Sauerstoffversorgung. So kann beispielsweise der Darm bis zu einem Blutdruck von 40 mmHg über eine Erhöhung der Sauerstoffextraktion aus der Rekrutierung mesenterialer Gefäße die fortwährende Versorgung mit Sauerstoff gewährleisten. Unterhalb dieses Wertes wird das Gewebe ischämisch, wobei die Ischämietoleranz des Intestinaltrakts lediglich bei 2 bis 3 Stunden liegt [7,8].
Es erscheint also zwingend notwendig bei möglichen Minderperfusionen der viszeralen Organe, auch durch iatrogene Okklusionen während einer Operation, den Aspekt „Zeit“ im Auge zu behalten oder alternativ bei langen komplexen Operationen die viszerale Perfusion beispielsweise mit einem ECMO-Bypass sicherzustellen.
Verschiedene Untersuchungen konnten die Relevanz der Malperfusion bei Typ B-Dissektionen zeigen. Gargiulo et al. fassten diese Ergebnisse zusammen und stellten eine Verbindung zwischen Durchblutungsstörungen der Beine und parallelen Durchblutungsstörungen der renalen und viszeralen Organe her [9]. Zwar wurden hier akute Typ B-Dissektionen betrachtet, es konnte aber somit während und nach der Dissektion über die Extremitäten eine Abschätzung der möglichen Organschäden gemacht werden.
Wie wichtig die Auseinandersetzung mit der Minderdurchblutung bei der Aortendissektion ist, stellten Sievers et al. in einer Untersuchung dar, nachdem sie die Dissektionen in A, B und non-A/non-B anhand des TEM-Systems klassifizierten. Während sich koronare Minderperfusionen lediglich bei Typ A-Dissektionen zeigten, waren viszerale oder iliacale Perfusonsdefizite in allen Klassifizierungen relevant [10]. Zwar beschäftigt sich der überwiegende Teil der Untersuchungen mit schon bestehenden Durchblutungsstörungen bei Aufnahme bzw. Diagnostik der Dissektion, die Folgen können aber auf eine lange intraoperative Minderperfusion übertragen werden. Alle Autor:innen heben die Dringlichkeit einer Intervention bei bestehender Minderperfusion hervor und die möglichst rasche Wiederherstellung der normalen Durchblutung. Das unterstreicht die Relevanz ein möglichst physiologisches Flussprofil in den distalen Gefäßbetten zu erhalten. Die derzeit verfügbaren Techniken zur pulsatilen Perfusion der unteren Extremitäten bei endovaskulären und offenen Aorteneingriffen sind heterogen und reichen von distalen Perfusionskanülen bei femoraler Kanülierung über axillofemorale Bypässe bis hin zu komplexen Shuntlösungen mit Schleusen oder zusätzlichen Pumpensystemen. Das hier vorgestellte CARL-System reiht sich in diese Gruppe ein. Es erlangt dann eine besondere Bedeutung, wenn die Daten zur Beinperfusion auf die Perfusion der viszeralen Organe übertragen werden und auch hier eine Pulsatilität Anwendung findet.
Schlussfolgerung
Bei langwierigen Gefäßoperationen ist der extrakorporale Bypass mittels ECMO zur Vermeidung von Perfusionsstörungen an Organen und Extremitäten eine mittlerweile an Zentren etablierte Option, um die postoperativen Komplikationsraten zu vermindern. Hauptaspekt ist dabei die Aufrechterhaltung einer Perfusion, wobei verschiedene technische Ansätze zur Beinperfusion – einschließlich alternativer pulsatiler Systeme – verfügbar sind. Durch die Entwicklung von Systemen mit pulsatilem Flussprofil könnte die bisherige Bypass-Perfusion um eine simulierte physiologische Mikrozirkulation erweitert werden. In dieser Kasuistik konnte, während einer 10-stündigen Multibranch-OP, gezeigt werden, dass eine über mehrere Stunden dauernde pulsatile Perfusion der unteren Extremität möglich und sicher ist. Darüber hinaus können Ischämie-Komplikationen über die notwendige Gefäß-Okklusion effektiv verhindert werden. In weiteren Anwendungen müsste das Verfahren verfeinert werden; anschließende Untersuchungen sollten zunächst die Beinperfusion systematisch mit anderen verfügbaren Techniken vergleichen und könnten danach eine Erweiterung auf andere Organbereiche, beispielsweise viszerale Endorgane, evaluieren.
Interessenkonflikt
Die Autoren haben keine finanziellen Interessen oder Beziehungen, die zu Interessenkonflikten führen können.
Herr Dr. Eike Gamon erhält Berater- und Vortragshonorare von der Firma Resuscitec und der Firma Becton Dickinson (BD).
Literatur
- Baća, I. et al: Vergleichende Studie über pulsatilen und kontinuierlichen Fluß während des extracorporalen Kreislaufs. Auswirkungen auf die Leberfunktion und endokrine Pankreassekretion. In: Linder, F., Röher, HD., Mittmann, U. (eds) Chirurgisches Forum ’79. Deutsche Gesellschaft für Chirurgie, vol 79. 1979, Springer, Berlin, Heidelberg. https://doi.org/10.1007/978-3-642-67291-0_10
- Hanke T, Gerdes A: Gibt es einen Vorteil der pulsatilen Perfusion gegenüber der nicht-pulsatilen Perfusion hinsichtlich der Morbidität, Mortalität oder weiterer Surrogatparameter?. In: Bartels, C., et al. Extrakorporale Zirkulation — wissenschaftlich begründet? 2001 Steinkopff, Heidelberg. https://doi.org/10.1007/978-3-662-21896-9_2
- Kalder J, Jalaie H, Greiner A, Jacobs MJ: A new shunting concept to prevent lower limb ischemia/ reperfusion injury in prolonged fenestrated stent-graft procedures. J Cardiovasc Surg (Torino). 2014 Apr;55(2 Suppl 1):183-5. PMID: 24796912.
- Neue OP-Methode in Dresden: ECMO-Einsatz unterstützt Austausch der Hauptschlagader, Kardiotechnik, German Journal of Perfusion 2015, Heft 4/2015, 24. Jahrgang, 104
- Coselli JS: The use of left heart bypass in the repair of thoracoabdominal aortic aneurysms: current techniques and results. Semin Thorac Cardiovasc Surg. 2003 Oct;15(4):326-32. doi: 10.1053/s1043-0679(03)00090-x. PMID: 14710373.
- Ghosh S, Roberts N, Firmin RK, Jameson J and Spyt TJ: Risk factors for intestinal ischaemia in cardiac surgical patients. European journal of cardiothoracic surgery: official journal of the European Association for Cardio-Thoracic Surgery2002. 21(3):411-416.
- Lange H: [Differential diagnostic significance of lactate in acute abdominal diseases]. Der Chirurg 1989; Zeitschrift fur alle Gebiete der operativen Medizen 60(5):356-360.
- Bradbury AW, Brittenden J, McBride K and Ruckley CV: Mesenteric ischaemia: a multidisciplinary approach. The British Journal of Surgery 1995; 82(11):1446-59.
- Gargiulo M, Bianchini Massoni C, Gallitto E, Freyrie A, Trimarchi S, Faggioli G, Stella A. Lower limb malperfusion in type B aortic dissection: a systematic review. Ann Cardiothorac Surg. 2014 Jul;3(4):351-67. doi: 10.3978/j.issn.2225-319X.2014.07.05. PMID: 25133098; PMCID: PMC4128931.
- Sievers HH, Rylski B, Czerny M, Baier ALM, Kreibich M, Siepe M, Beyersdorf F: Aortic dissection reconsidered: type, entry site, malperfusion classification adding clarity and enabling outcome prediction. Interact Cardiovasc Thorac Surg. 2020 Mar 1;30(3):451-457. doi: 10.1093/icvts/ivz281. PMID: 31755925.







