Einleitung
Die Organtransplantation ist eine lebensrettende Maßnahme für Patienten, die an akutem oder chronischem Organversagen im Endstadium leiden [1]. Der anhaltende Mangel an Spenderorganen und die wachsende Zahl von Patienten auf den Wartelisten stellt eine erhebliche Herausforderung für die Patientenversorgung dar [2,3]. Um der Diskrepanz zwischen Organangebot und -nachfrage entgegenzuwirken, wurde die Organspende nach dem Kreislaufstillstand (DCD) [4] und die Verwendung von Spendern mit erweiterten Spenderkriterien (ECD) [5] in die klinische Routine integriert. Hierdurch kann eine Reduktion der Wartelistensterblichkeit erreicht werden [6,7], jedoch sind beide Maßnahmen mit einem schlechteren klinischen Outcome aufgrund kompromittierter Organqualität assoziiert [8]. Seit der Jahrtausendwende hat das Interesse an der Organkonservierung mittels Maschinenperfusion (MP) stark zugenommen, angetrieben durch die Notwendigkeit, die Transplantationsergebnisse zu verbessern, sowie durch technologische Innovationen und ein wachsendes Verständnis zur Organerhaltung [2].
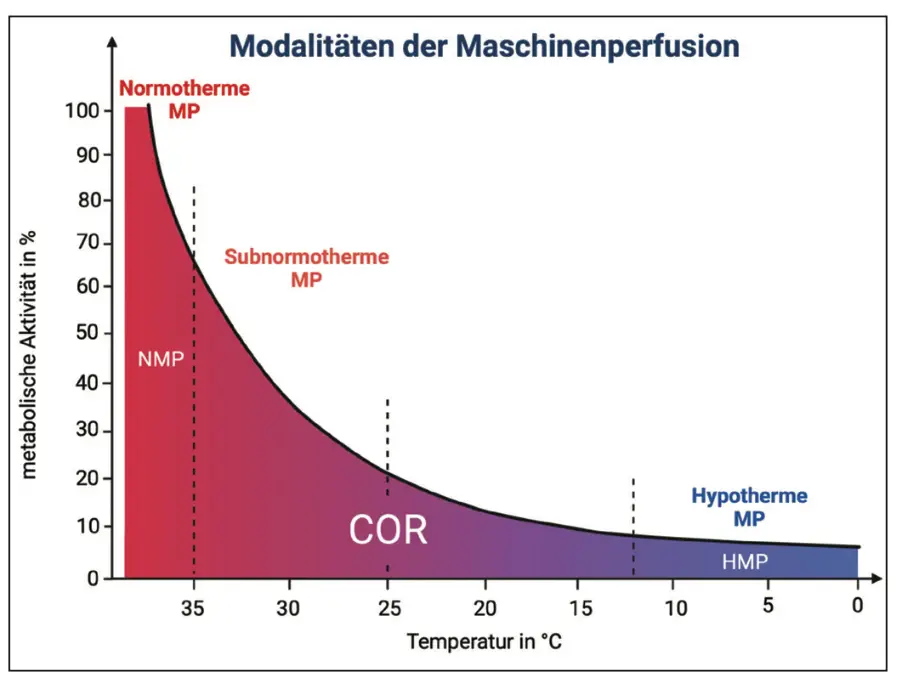
Die Maschinenperfusion (MP) ist eine dynamische Form der Organkonservierung, bei der die physiologischen Bedingungen des Körpers imitiert und Beschädigungen der Organe in der kritischen Phase zwischen Entnahme und Transplantation vorgebeugt werden [9,10]. Seit den Anfängen hat sich die Technik der maschinellen Perfusion umfassend weiterentwickelt und diversifiziert. Ihre Anwendung kann sowohl extra- als auch intrakorporal erfolgen, transportabel (upfront) sowie nicht-transportabel (back-to-base/end-ischämisch) und als normotherme, subnormotherme oder hypotherme Perfusion durchgeführt werden [11–14]. Trotz der technischen Fortschritte steht die Umsetzung von MP in der klinischen Routine vor Herausforderungen, einschließlich des Bedarfs an Spezialausrüstung, geschultem Personal und standardisierten Protokollen [15]. Darüber hinaus ist die Kosteneffizienz des Einsatzes von MP nach wie vor umstritten [15]. Diese Übersichtsarbeit zielt darauf ab, die unterschiedlichen Anwendungsmodalitäten der Maschinenperfusion sowie die Evidenz ihres klinischen Einsatzes in den unterschiedlichen Organsystemen darzustellen.
Aktuelle Perfusionsmodalitäten in der Organtransplantation
Normothermic Regional Perfusion (NRP)
Die normotherme regionale Perfusion kommt im Gegensatz zu den Verfahren der Ex-vivo-Maschinenperfusion (s. u.) im Körper des Spenders und während der Organentnahme selbst zum Einsatz. Diese Methode der In-situ-Perfusion wird ausschließlich bei der Organspende nach Kreislauftod (donation after circulatory death – DCD) angewendet und dient primär dazu, die unterbrochene Eigenperfusion des Organs im Spender temporär zu ersetzen [16]. NRP wird sowohl für abdominelle als auch für thorakale Spenderorgane weltweit zunehmend als sichere Alternative zur In-situ-Kühlung und dem sogenannten rapid procurement eingesetzt. In der Lebertransplantation hat sich gezeigt, dass die NRP bei der kontrollierten Spende nach Kreislaufstillstand im Vergleich zur In-situ-Kältekonservierung zu einer Verringerung von postoperativen Komplikationen, insbesondere biliärer Komplikationen nach DCD führt [17]. Ebenso konnte in zwei kürzlich veröffentlichten Studien eine verbesserte ein- und zwei-Jahres-Transplantatfunktion [18] sowie eine Reduktion der Rate an verzögerter Transplantatfunktion (delayed graft function – DGF) [19] nach Nierentransplantationen gezeigt werden, die unter einer NRP-Anwendung entnommen wurden, im Vergleich zur konventionellen Organentnahme [20,21].
Verfahren der Ex-vivo-Maschinenperfusion
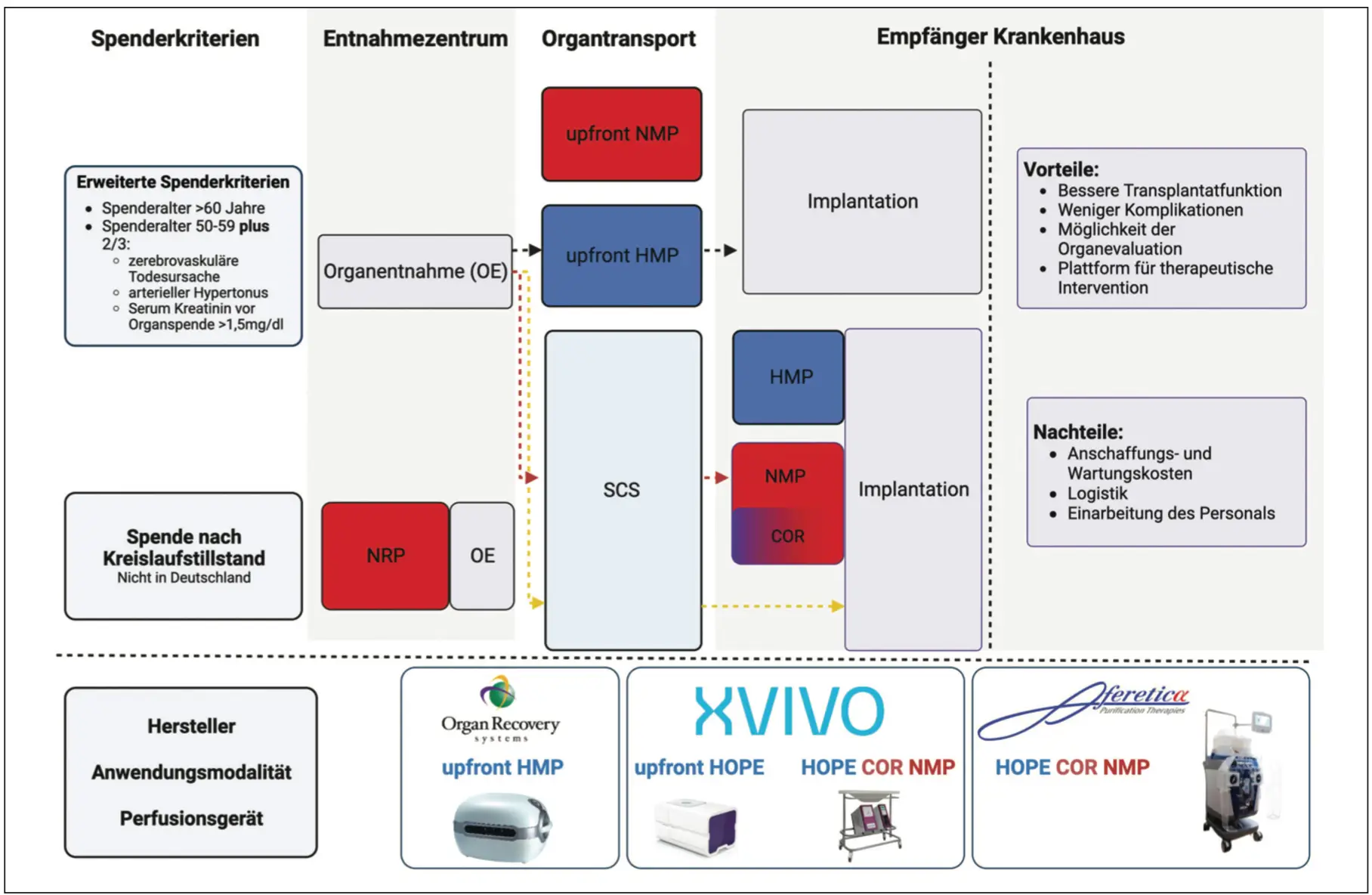
Die maschinelle Perfusion von Spenderorganen außerhalb des Körpers (Ex-vivo-Organperfusion) kann entweder kontinuierlich (upfront), von der Entnahme des Organs bis zu seiner Implantation, oder endischäm, ab Ankunft des Spenderorgans im Transplantationszentrum, durchgeführt werden. Zwei am häufigsten eingesetzten Perfusionstechniken sind hierbei die normotherme (NMP) und die hypotherme Maschinenperfusi- on (HMP) – siehe Abbildung 1 und 2.
Normotherme Maschinenperfusion (NMP)
Im Rahmen der NMP werden Spenderorgane bei Temperaturen von 36–37 °C mit einer speziellen Perfusionslösung per- fundiert und damit unter annähernd physiologischen Bedingungen konserviert. Bei den hierfür zum Einsatz kommenden Perfusionslösungen (Priming) können entweder azelluläre Speziallösungen oder ein zellbasiertes Priming aus Erythrozytenkonzentraten, kolloidhaltiger Lösungen und Medikamenten angewendet werden. Hierdurch kann der Organmetabolismus reaktiviert und die zellulären Energiespeicher aufgefüllt werden [22]. Die Imitation der Organfunktion außerhalb des menschlichen Körpers ermöglicht es die Qualität der Spenderorgane vor der Transplantation zu evaluieren und marginale Spenderorgane vor einer jeweiligen Transplantation zu bewerten. Die hierdurch erreichte Steigerung der Spenderorganausschöpfung aus dem zur Verfügung stehenden Spenderorganpool kann zur Steigerung der Transplantationszahlen beitragen und hierdurch eine Reduktion der Wartelistenmortalität bedingen [23]. NMP wird bislang bei der Transplantation von Leber, Herz, Lunge und Niere eingesetzt. In präklinischen Studien konnte durch die Optimierung des Kreislaufsystems, der Primingzusammensetzung und der Überwachungsmöglichkeiten durch geeignete Messtechnik die Konservierungsdauer auf mehrere Tage ausgeweitet werden [24]. Außerdem eröffnen sich neue Einsatzmöglichkeiten bei weiteren Organsystemen, einschließlich Pankreas-, Darm-, Gebärmutter-, Eierstock- und vaskularisierten Lappentransplantaten [25–28]. Neben der Funktion als Konservierungsmethode fungiert die NMP ebenfalls als Plattform für die biomedizinische Forschung, da sie ein realistisches Modell für die Untersuchung der Organphysiologie, -pathologie und therapeutischer Interventionen ermöglicht [29]. So können neuartige Therapien, wie die Infusion mesenchymaler Stammzellen (MSC) während der Perfusion eingesetzt werden, um die Organqualität zu verbessern und Reparaturprozesse zu fördern [30–33].
Hypotherme Maschinenperfusion (HMP)
Die erste klinische Anwendung einer Maschinenperfusion zur Organkonservierung erfolgte bereits 1968 durch Folkert
O. Belzer in Form der hypothermen maschinellen Perfusion – damals zur Konservierung eines Nierentransplantates [34]. Während der HMP wird das Spenderorgan mit einer kalten Konservierungslösung (1–10 °C) durchspült, was zur Verlangsamung des zellulären Stoffwechsels und des Energieverbrauches führt. Darüber hinaus fördert die Perfusion des Organs den Abtransport zytotoxischer Metabolite und wirkt über mechanische Stimulation des Endothels der Expression proinflammatorischer Proteine wie Zytokine, Vimentin, Endothelin, Toll-like-Rezeptor 4 und High-Mobility Group Box 1 (HMGB1)-Genen entgegen [35–39]. Angesichts der Rolle von Hypoxie und mitochondrialer Energieverarmung bei der Entstehung des Ischämie-Reperfusionsschadens wurde außer- dem eine Oxygenierung in die Perfusionskreisläufe integriert [40–42]. Die Perfusion des Organs mit oxygenierter Flüssigkeit unter hypothermen Bedingungen (HOPE) ermöglicht die Wiederherstellung der zellulären Energiespeicher und übt dadurch einen schützenden Einfluss auf den mitochondrialen Stoffwechsel und die Entstehung von Sauerstoffradikalen aus [21,22]. Das Zusammenwirken der verschiedenen Mechanismen führt zu einer wesentlichen Reduktion des Ischämie-Reperfusionsschadens in HOPE-therapierten Organen, was sich für die Organsysteme der Niere, Leber, Herz und Lunge in einem besseren klinischen Outcome nach der Transplantation widerspiegelt [43–48]. Zusätzlich zu diesem therapeutischen Effekt der HOPE-Anwendung konnte in aktuellen Studien auch die Möglichkeit einer Viabilitätsprüfung mittels hypothermer Maschinenperfusion – trotz der reduzierten Stoffwechselaktivität – in Lebertransplantaten gezeigt werden. [49]
Ischämiefreie Organtransplantation (IFOT)
Die ischämiefreie Organtransplantation ist ein neuartiger Ansatz, um den Ischämie-Reperfusionsschaden während einer Organtransplantation vollständig zu umgehen. Hierfür wird das Organ bereits während der Entnahme im Körper des Spenders kanüliert und mit einer Ex-vivo-NMP-Maschine verbunden, so dass während der Organentnahme eine kontinuierliche Blutversorgung des Gewebes gewährleistet ist. Während der Implantation kann das Organ unter anhaltender Perfusion zunächst im Situs des Empfängers platziert und dann schrittweise an seine Blutversorgung angeschlossen werden, ohne eine Gewebsischämie durch Wegfallen der Perfusion zu provozieren [50]. Im Jahr 2021 wurde von Guo et al. eine nicht-randomisierte, kontrollierte Studie zur ischämiefreien Lebertransplantation (IFLT) veröffentlicht, bei der die IFLT-Gruppe im Vergleich zur traditionellen Lebertransplantationsgruppe (CLT) eine signifikant niedrigere Rate an früher Transplantat-Dysfunktionen (early allograft dysfunction – EAD) und niedrigere Leberfunktionsparameter aufwies [50]. Den vielversprechenden klinischen Ergebnissen der IFLT stehen jedoch erhebliche Einschränkungen in Bezug auf den logistischen und technischen Aufwand gegenüber, die ihre flächendeckende Anwendbarkeit weitgehend einschränken.
Controlled Oxygenated Rewarming (COR)
Eine weitere Perfusionstechnik ist die kontrollierte oxygenierte Wiedererwärmung (controlled oxygenated rewarming – COR), die nach dem Organtransport mittels statischer Kaltlagerung oder einer hypothermen Anwendung eingesetzt werden kann [51]. Im Gegensatz zur endischämen NMP wird das Spenderorgan nach Anschluss an das Perfusionssystem kleinschrittig durch Anheben der Perfusionstemperatur und des Perfusionsdruckes erwärmt. Durch den kontrollierten Temperaturanstieg kann der sogenannte rewarming injury, der durch eine plötzliche Erhöhung der Gewebetemperatur mutmaßlich verursacht wird, reduziert werden [52–54]. Klinische Daten zu dieser neuen Perfusionsform sind begrenzt und beschränken sich auf die Transplantation der Niere und Leber. Eine Pilotstudie zur Anwendung bei Nierentransplantaten (n = 6) zeigte, dass durch COR vorbehandelte Spendernieren im Vergleich zur Kontrollgruppe (statische kalte Lagerung – SCS) eine bessere frühe Transplantatfunktion aufweisen [55].
In einer kürzlich veröffentlichten randomisierten, kontrollierten Studie zeigten Spenderlebern, die mit COR behandelt wurden, im Vergleich zur SCS eine bessere Leberfunktion, gemessen am LiMAX unmittelbar nach der Lebertransplantation, einem Leberfunktionstest, bei dem die Abbaufunktion der Leber quantifiziert werden kann [51]. Weitere klinischen Stu- dien sind jedoch notwendig, um den tatsächlichen Mehrwert von COR gegenüber der normothermen Maschinenperfusion abzugrenzen.
Maschinenperfusion in verschiedenen Organsystemen
Herz: Derzeit ist die statische Kaltlagerung (SCS) der Goldstandard zur Konservierung von Spenderherzen [56], wobei verlängerte Ischämiezeiten nach wie vor eine Hauptursache für Transplantatversagen darstellen [56]. Die klinische Evidenz zur Anwendung von Maschinenperfusion zur Konservierung von Spenderherzen ist aktuell qualitativ und quantitativ begrenzt. In einer kürzlich veröffentlichten Übersichtsarbeit von Quin et al. wurden 32 Studien zur normothermen und drei zur hypothermen Maschinenperfusion bei Herztransplantationen zusammengefasst. Hierbei konnte für beide Perfusionsformen kein klarer klinischer Benefit gegenüber der Kaltlagerung gezeigt werden [56]. Eine aktuelle randomisierte, kontrollierte Studie (n = 229) zeigte eine 44 %ige Risikoreduktion bezüglich Herzversagens, Herztod und Organabstoßung innerhalb 30 Tage nach HTX, die mit dem Einsatz von HOPE zur Konservierung von Spenderherzen assoziiert war, jedoch ohne dass ein signifikanter Unterschied zwischen beiden Versuchsgruppen vorlag [48].
Lunge: Die Ex-vivo-Lungenperfusion (EVLP) wurde erstmals 2006 von der Gruppe von Stig Steen in Lund, Schweden, eingesetzt [57], und ist seitdem von verschiedenen Zentren weltweit übernommen worden. Zusätzlich zur normothermen Perfusion, wird die Spenderlunge vor der Transplantation mehrere Stunden lang bei Körpertemperatur beatmet [58]. Weltweit sind mehrere EVLP-Protokolle im Einsatz, darunter Protokolle von Toronto, Lund und Organ Care Systems (OCS), die sich primär bezüglich der Zusammensetzung der Perfusionslösung, dem pulmonal-arteriellen Druck, dem Druck im linken Vorhof und den Beatmungseinstellungen unterscheiden. Als Perfusionslösung kann sowohl eine zelluläre als auch azelluläre Lösungen verwendet werden [59]. Azelluläre Lösungen senken das Risiko einer Hämolyse und einer thrombotischen Lungenverletzung, während zelluläre Lösungen eine bessere Oxygenierung und ein Monitoring ermöglichen [60]. Durch das Organassessment mittels EVLP können mehr marginale Spenderlungen sicher transplantiert werden [61,62]. Die Technik ermöglicht auch die Behandlung von Infektionen und anderen Lungenerkrankungen vor der Transplantation, was eine zusätzliche Erweiterung des Spenderpools möglich werden lässt [60]. Das optimale EVLP-Protokoll ist jedoch nach wie vor Gegenstand laufender Forschungsarbeiten [60].
Niere: Trotz der bereits frühen Anwendung von maschinengestützter Organkonservierung in der Nierentransplantation etablierte sich auch für die Konservierung von Spendernieren zunächst die statische Kaltlagerung aufgrund ihrer Kosteneffizienz und technischen Einfachheit als Methode der Wahl [63]. Erste klinische Evidenz zur Überlegenheit von hypothermer Maschinenperfusion gegenüber der SCS wurde 2009 durch die Ergebnisse einer multizentrischen, randomisierten Studie von Moers et al. sichtbar [64]. Die Gruppe zeigte für die Nierentransplantation von postmortalen Spendern, dass kontinuierlich perfundierte Organe ein reduziertes Risiko der verzögerten Transplantatfunktion (DGF) sowie ein verbessertes Transplantatüberleben (graft survival) ein Jahr nach Transplantation erreichten [64]. Der therapeutische Benefit der kontinuierlichen HMP konnte in weiteren klinischen Studien und Metanalysen sowohl für Nierenspende nach DCD also auch nach Hirntod-Spende (donation after brain death – DBD) bestätigt und die Kosteneffizienz für den europäischen und US-amerikanischen Markt gezeigt werden [43,47,65,66]. Jochmans et al. verglichen im Rahmen des COMPARE-Trials den Effekt hypothermer Maschinenperfusion mit und ohne Beimengung von Sauerstoff zur Konservierung von DCD-Nieren, wobei sich in der Gruppe der zusätzlich oxygenierten Nieren weniger postoperative Komplikationen und Transplantatversagen zeigten [67]. Interessanterweise scheint sich der therapeutische Effekt von HMP auf die kontinuierliche Anwendung zu beschränken und beim Einsatz als endischäme Perfusion gegenüber der statischen Kaltlagerung nicht vorhanden zu sein [68]. Der Einsatz von normothermer Maschinenperfusion zur Konservierung von Spendernieren ist im Vergleich zur hypothermen Anwendung kaum untersucht. 2023 wurde die derzeit einzige randomisiert kontrollierte Studie über endischämische NMP versus statische Kaltlagerung zur Konservierung von DCD-Nieren veröffentlicht. Dabei konnte die sichere NMP-Anwendung gezeigt werden [69]. Diese Evidenzlücke wird aktuell durch eine vom Bundesministerium für Bildung und Forschung (BMBF) geförderte Studie aus Heidelberg adressiert. Die NMP-DBD-Studie untersucht weltweit erstmalig den Effekt endischämischer normothermer Maschinenperfusion auf marginale Spendernieren, welche die extended criteria donation (ECD) erfüllen, nach Hirntodspende im Vergleich zur SCS und befindet sich ab 2025 in der Rekrutierungsphase (clinicaltrials.gov: NCT05031052). Hinweise für einen therapeutischen Benefit der normothermen maschinellen Perfusion zur Konservierung von Nieren beschränken sich derzeit auf Ergebnisse aus präklinischen Studien [70–72]. Neuere Perfusionstechniken, wie die oben erwähnte kontrollierte, oxygenierte Erwärmung (COR), wurden in der Nierentransplantation bislang nur als Pilotstudien exploriert [55]. Mehrere internationale Forschungsvorhaben untersuchen derweil die kombinierte Anwendung der hypothermen und normothermen Maschinenperfusion (clinicaltrials.gov: NCT05782543 und NCT04882254).
Leber: Die Maschinenperfusion von Spenderlebern wurde klinisch 2004 zum ersten Mal in Form der hypothermen Maschinenperfusion untersucht [73]. In den darauffolgenden Jahren konnte in mehreren randomisierten, kontrollierten Studien ein positiver Effekt der hypothermen, oxygenierten Maschinenperfusion in endischämer Anwendung auf die postoperative Komplikationsrate sowie Transplantatfunktion und -überleben für sowohl DCD- [74] als auch ECD-Lebern [45,75,76] gezeigt werden. Ein entscheidender Vorteil des HOPE-Einsatzes ist der präventive Effekt auf die Entstehung von Gallenwegstrikturen, welche als schwerwiegende Komplikation insbesondere bei
DCD-Lebern auftreten können und häufig mit der Notwendigkeit einer Retransplantation einhergehen [74]. Diese Ergebnisse konnten nicht zuletzt im Rahmen der ersten Metaanalyse in der Maschinenperfusion zur Lebertransplantation bestätigt werden, sondern wurden auch in den ersten Langzeitergebnissen dargestellt [46,75]. Die hypotherme Perfusion erfolgt in dem Organsystem der Leber entweder nur über die Portalvene (HOPE) oder die Pfortader und Arterie (Dual-HOPE). Neben dem therapeutischen Effekt der HOPE-Anwendung scheint es zudem möglich zu sein, die Qualität einer Spenderleber durch die Bestimmung von Flavinmononukleotid (FMN) im Perfusat zu evaluieren [77]. FMN wird als Folge von mitochondrialem Schaden freigesetzt und seine Konzentration im Perfusat korreliert mit dem postoperativen Auftreten von biliären Strikturen und von Transplantatverlust [49]. Die Möglichkeit der„On-pump“-Organevaluation ist bislang primär Domäne der NMP. Relevante Parameter umfassen hierbei die Gallenproduktion, die Laktat-Clearance und den pH-Wert von Perfusat und Galle während der Perfusion [78,79]. Das Verwenden von NMP als Assessmentplattform für Risikoorgane ermöglicht es mehr Organe als transplantabel zu bewerten und Transplantationszahlen zu erhöhen [80,81]. Darüber hinaus scheint NMP ebenfalls den Ischämie-Reperfusionsschaden in den Organen und eine Organdysfunktion nach der Transplantation (EAD) zu verringern [46,80]. Die Ergebnisse der aktuell veröffentlichen RCTs beziehen sich jedoch auf die kontinuierliche Anwendung von NMP (cNMP), welche aufgrund ihres erheblichen logistischen und technischen Aufwandes mit einer hohen Kostenlast einhergehen und die Frage der Kosteneffizienz deutlich werden lässt [80–82]. Derzeit wird die Fragestellung der endischämen NMP in der Lebertransplantation sowie der direkte Vergleich von HOPE zur NMP im Rahmen der internationalen, randomisiert kontrollierten HOPE-NMP-Studie untersucht (clinicaltrials.gov: NCT04644744). Um den therapeutischen Effekt der HOPE mit der Möglichkeit der Organevaluation während der NMP zu vereinen, können beide Techniken miteinander kombiniert werden [83]. Auch die Kombination von normothermer regionaler Maschinenperfusion mit endischämer Maschinenperfusion wurde bereits erfolgreich zur Konservierung von Hochrisiko-Spenderorganen angewandt [84].
Pankreas: Die Transplantation der Bauchspeicheldrüse stellt für Patienten mit Typ-I-Diabetes eine Möglichkeit der endgültigen Heilung dar und verbessert sowohl das Langzeitüberleben als auch die Lebensqualität der Patienten [85]. Im Gegensatz zu den Organsystemen der Leber, Niere, Lunge und Herz beschränkt sich der Einsatz von Maschinenperfusion zur Konservierung von Pankreastransplantaten weitestgehend auf die experimentelle Anwendung. Die bisherige präklinische Evidenz zeigt auch hier einen therapeutischen Effekt von HOPE auf den Ischämie-Reperfusionsschaden und Entzündungsprozesse im Pankreasgewebe nach Reperfusion auf [86,87]. Ebenso ist die Anwendung von endischämer NMP zur Konservierung von humanen Pankreastransplantaten Gegenstand aktueller Forschungsbemühungen [88]. Die Abwesenheit klinischer Studien lässt jedoch bisweilen keine Aussage über den klinischen Mehrwert von Maschinenperfusion in der Pankreastransplantation zu.
Schlussfolgerungen
Der Einsatz von Maschinenperfusion stellt einen Paradigmenwechsel in der Organerhaltung dar. Mit der wachsenden Evidenz für ihre therapeutische Wirksamkeit und der Erweiterung ihrer Einsatzmöglichkeiten ist eine Entwicklung zum neuen Goldstandard in der Konservierung für die solide Organtransplantation absehbar. Zukünftige Forschungsarbeiten sollten sich auf die Kosten-Nutzen-Analyse, die langfristigen, klinischen Vorteile und die Integration mit fortschrittlichen Biotechnologien konzentrieren. Mit der zunehmenden Nutzung der Maschinenperfusion bzw. Ex-vivo-Organperfusion in der Transplantationsmedizin eröffnet sich eine neue Domäne der multidisziplinären Zusammenarbeit zwischen Transplantationschirurgen und Perfusionisten, die für die flächendeckende Implementierung dieser Technologie in Zukunft von entscheidender Bedeutung sein wird.
Wissenschaftlicher Kurzlebenslauf
Professor Dr. med. Georg Lurje
Stellvertretender ärztlicher Direktor und leitender Oberarzt Sektionsleiter Leberchirurgie und viszerale Transplantationschirurgie
Universitätsklinikum Heidelberg
Klinik für Allgemein-, Viszeral- und Transplantationschirurgie
Klinische Schwerpunkte
- minimal-invasive Chirurgie
- hepatobiliäre und Pankreaschirurgie (HPB-Chirurgie)
- Transplantationschirurgie
Gremienarbeit
Seit 2023 Mitglied der Ständigen Kommission Organtransplantation (StäKO) der Bundesärztekammer
Seit 2021 Vorstandsmitglied Eurotransplant (Council of Medicine and Science – section liver)
Seit 2023 Federführung der Richtlinien Arbeitsgruppe Niere der Ständigen Kommission Organtransplantation (StäKO, Bundesärztekammer)
Seit 2022 Vorsitzender der Chirurgischen Arbeitsgemeinschaft Transplantation (CAT) der Deutschen Gesellschaft für Allgemein- und Viszeralchirurgie (DGAV)
Seit 2022 Medizinischer Sachverständiger der Bundesärztekammer (Ex-vivo-Maschinenperfusion abdomineller Spenderorgane)
Seit 2022 Medizinischer Sachverständiger der Bundesärztekammer zur Prüfung der Transplantationszentren
Klinische Studien (als Hauptprüfarzt und Leiter der klinischen Studie)
Seit 2025: NMP-DBD Studie (NCT05031052)
Seit 2021: HOPE-NMP Studie (NCT04644744)
2016–2020: HOPE ECD-DBD Studie (Ann Surg 2021, NCT03124641)







