Einleitung
Implantierbare Defibrillatoren (ICD, Implantable Cardioverter Defibrillators) nehmen eine wesentliche Stellung in der Behandlung von Patient:innen mit einem hohen Risiko für den plötzlichen Herztod ein – oder für jene die diesen überlebt haben. ICDs sind dafür konzipiert, lebensbedrohliche ventrikuläre Arrhythmien wie ventrikuläre Tachykardien (VT) und Kammerflimmern (VF) zu erkennen (Sensing) und zu behandeln (Defibrillation oder antitachykardes Pacing – ATP). Ein ICD kann das gesamte Spektrum der zum plötzlichen Herztod führenden Arrhythmien behandeln. Die koronare Herzkrankheit stellt die Hauptursache dar und ist in bis zu 80 % der Fälle prävalent, während weitere 10–15 % auf nicht-ischämische Kardiomyopathien (KMP) zurückzuführen sind. Hierbei repräsentiert die dilatative Kardiomyopathie (DKMP) neben der hypertrophen KMP, der arrhythmogenen rechtsventrikulären KMP, dem Long-QT-Syndrom, der familiären katecholaminergen polymorphen ventrikulären Tachykardie und dem Brugada-Syndrom den größten Anteil. Erworbene und erblich bedingte Erkrankungen machen die verbleibenden 5–10 % der Fälle aus. Seit den ersten gepoolten Analysen, die einen fast 30 %igen Überlebensvorteil für ICD-Träger durch die bloße Reduktion arrhythmischer Todesfälle zeigte, ist die ICD-Therapie ein Eckpfeiler der antitachykarden Therapie [1]. Die Herausforderung in der Nutzung der ICDs liegt in der differenzierten Indikationsstellung und der individuellen Programmierung. Jüngsten Anlass zum Überdenken des bisherigen Status Quo bot eine Metaanalyse, die eine reduzierte LVEF als wesentlichen Parameter zur Risikostratifizierung für einen plötzlichen Herztod entkräftete [2]. Über die letzten drei Dekaden hatte sich der Eindruck eines deutlichen präventiven Nutzens bei Herzinsuffizienzpatient:innen mit einer linksventrikulären Ejektionsfraktion (LVEF) ≤35 % etabliert und wurde erst 2020 relativiert. Grund für teils widersprüchliche Ergebnisse mögen unterschiedliche Ätiologien der Herzinsuffizienzen (ischämisch vs. nicht-ischämisch) sein [3,4].
Dieser Artikel bietet eine Übersicht über die verschiedenen Konfigurationen, die wesentlichen Programmierungsparameter, die aktuellen leitliniengerechten Indikationen und die neuesten Entwicklungen auf diesem Gebiet der ICDs. An entsprechenden Stellen sind Empfehlungsklassen und deren Evidenzgrade gemäß den 2022 ESC-Leitlinien hinterlegt [5].
Entscheidungsfindung zur ICD-Therapie
Im Rahmen der Vorbereitung auf eine ICD-Therapie ist es von entscheidender Bedeutung die Lebenserwartung, die Lebensqualität und bestehenden Komorbiditäten zu berücksichtigen. Diese Aspekte sind mit dem Patienten zu besprechen und auch fortwährend zu reevaluieren, um im Bedarfsfall Downgrades im Rahmen von Aggregatwechseln in Erwägung zu ziehen. Die Implantation eines ICDs wird nur bei Patient:innen empfohlen, bei denen eine Überlebensaussicht von mehr als einem Jahr besteht (Klasse I, Level C). Generell muss das Risiko eines plötzlichen Herztods gegen das individuelle Risiko eines nicht-arrhythmischen Todes abgewogen werden.
Ärzte sollten potenzielle ICD-Kandidaten in einen gemeinsamen Entscheidungsfindungsprozess mit einbeziehen. Hierbei sollten insbesondere Komplikationen wie inadäquate Schockabgaben, Sondenfrakturen oder geräteassoziierte Infektionen angesprochen werden und auch alternative Device- bzw. medikamentöse Therapieoptionen sowie deren Erfolgsraten dargestellt werden.
Funktionelle Konfigurationen
Je nach klinischem Bedarf gibt es unter- schiedliche Sondenkonfigurationen:
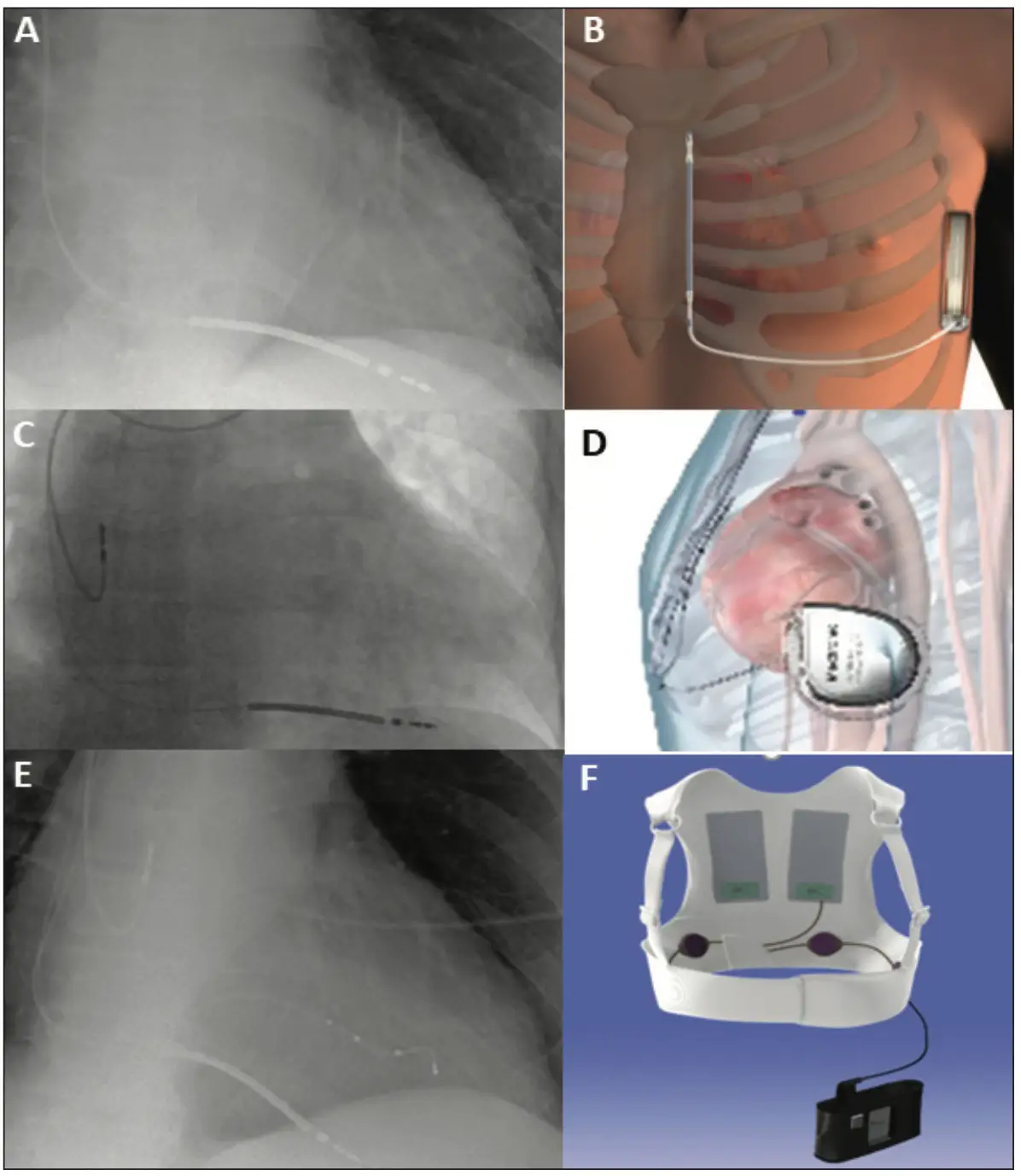
- Einkammer-Systeme (VR-ICD): Eine Schocksonde im rechten Ventrikel. Bei Patient:innen ohne aktuelle oder erwartete Indikation für eine atriale oder AV-sequenzielle Stimulation wird ein VR-ICD gegenüber einem DR- ICD empfohlen, da das Risiko gerätebedingter Komplikationen geringer ist (Klasse I, Level A). Diese Systeme sind für Patient:innen geeignet, die entweder einen ausschließlichen Schutz vor dem plötzlichen Herztod benötigen oder ausschließlich eine ventrikuläre Stimulation benötigen (Abb.1A).
- Zweikammer-Systeme (DR-ICD): Zusätzliche Sonde im rechten Vorhof für eine atriale- oder AV-sequenzielle Stimulation bei AV-Blockierungen. Diese Kombination bietet weiterhin die Option zur Therapie von Sinusknotenerkrankungen, wie dem Sick-Sinus-Syndrom oder einem Sinusarrest, bzw. binodaler Erkrankungen. Allerdings wird empfohlen, bei Patient:innen ohne ventrikuläre Stimulationspflicht bzw. Notwendigkeit zur antibradykarden Therapie den Stimulationsanteil auf ein Minimum zu beschränken (Klasse I, Level A) (Abb.1C).
- Kardiale Resynchronisationstherapie (CRT-D): Eine zusätzliche linksventrikuläre Sonde zur Verbesserung der ventrikulären Koordination. Besteht die Indikation zur ICD-Therapie (CM, EF < 35%) bei weiterhin asynchroner Ventrikelkontraktion und Vorliegen eines Linksschenkelblocks (LSB) mit einer QRS-Breite >150 ms, so wird empfohlen zu prüfen, ob der Patient von einem CRT-Defibrillator profitieren könnte (Klasse I, Level C) (Abb.1E).
- Subkutane ICDs: Der subkutane ICD stellt eine Alternative zum transvenösen ICD dar, wenn eine antibradykarde Stimulationstherapie, eine kardiale Resynchronisation oder die Abgabe von ATPs nicht zu erwarten sind bzw. ernste Argumente zur Vermeidung intravasal gelegener Elektroden vorliegen (Klasse IIa, Level B. (Abb.1B).
- Extravaskuläre ICDs (EV-ICDs) sind eine alternative Entwicklung zu subkutanen ICDs, die die Vorteile von subkutanen ICDs (s-ICDs) und transvenösen ICDs vereinen sollen. Hierzu wird die spezielle Elektrode (1) intrathorakal, aber extravaskulär platziert und ermöglicht im Unterschied zu den S-ICDs (2) durch ihre retrosternale Sondenlage antitachikardes Pacing (ATP) und eine antibradykarde Stimulation (Abb.1D, 3A-C).
- Defibrillationswesten (sog. „Wearables“/WCD – wearable cardioverter/defibrillator): Die Defibrillationsweste ist für erwachsene Patient:innen geeignet, die ein vermutet hohes Risiko für den plötzlichen Herztod aufweisen. Hierbei kommen einerseits Patient:innen nach einem akuten Myokardinfarkt oder einer noch nicht abgeschlossenen Diagnostik (z. B. Ionenkanalerkrankungen) in Betracht, wie auch andererseits Patient:innen, die sich noch in der Phase einer optimalen medikamentösen Therapie (OMT) nach Myokardinfarkt (Klasse IIa, Level C) befinden. So konnten durch eine effektivere medikamentöse Therapie unter einem temporären WCD-Schutz die ICD-Implantationszahlen auch deutlich reduziert werden [6,7] (Abb.1F). Nicht zuletzt ist die Weste bei Patient:innen mit sekundärprophylaktischer ICD-Indikation indiziert, insbesondere bei vorübergehenden Kontraindikationen wie ICD-Infektionen oder Endoplastitis.
Indikationen
Primärprophylaxe
Die Primärprophylaxe zielt darauf ab, den plötzlichen Herztod bei Patient:innen ohne vorherige arrhythmische Ereignisse zu verhindern, die ein hohes Risiko für ventrikuläre Arrhythmien aufweisen. Die ersten Wochen nach einem Myokardinfarkt stellen das höchste Risiko für einen plötzlichen Herztod dar, insbesondere bei Patient:innen mit eingeschränkter LVEF [6]. Allerdings konnten Studien bereits vor 20 Jahren aufzeigen, dass frühzeitig prophylaktisch implantierte ICDs innerhalb der ersten 40 Tage nach einem Myokardinfarkt die Mortalität von Patient:innen mit reduzierter LVEF nicht reduzieren konnten [8,10]. Die noch laufende randomisierte PROTECT-ICD-Studie untersucht nun, ob die induzierbare Tachyarrhythmie ein Stratifizierungsparameter für eine ICD-Implantation bei Patient:innen mit eingeschränkter EF in der frühen Phase nach einem STEMI sein könnte. Die abschließende Indikation für eine prophylaktische ICD-Implantation sollte daher erst nach dem Post-Infarkt-Remodelling, also nach den ersten 6 Wochen bei Patient:innen mit einer prästationären LVEF ≤40 % erfolgen [11].
Herzinsuffizienz mit reduzierter Ejektionsfraktion (HFrEF)
Es geht um Patient:innen mit einer linksventrikulären Ejektionsfraktion (LVEF) von ≤35 % trotz optimaler medikamentöser Therapie. In diesem Patient:innenklientel sollte eine primärpräventive Therapiezone erst bei ≥188 Schlägen pro Minute beginnen (Klasse I, Level A).
Patient:innen mit koronarer Herzkrankheit
Etwa 40 Tage nach einem ST-Hebungsinfarkt (STEMI) weisen etwa 5 % der Patient:innen eine linksventrikuläre Ejektionsfraktion (LVEF) von ≤35 % auf. Diese Patient:innen haben ein erhöhtes Risiko für einen plötzlichen Herztod und sollten während der OMT bis zur finalen Diagnosestellung einen WCD-Schutz erhalten [12].
Empfehlungen:
- Eine ICD-Therapie wird bei Patient:innen mit KHK, symptomatischer Herzinsuffizienz (NYHA-Klasse II– III) und einer LVEF von ≤ 35 % trotz OMT von mindestens 3 Monaten empfohlen (Klasse I, Level A).
- Eine ICD-Therapie sollte bei Patient:innen mit KHK, NYHA-Klasse I und LVEF ≤30 % trotz ≥3 Monaten OMT in Betracht gezogen werden (Klasse IIa, Level B).
Bei Patient:innen mit koronarer Herzkrankheit, einer reduzierten LVEF (≤40 %) und asymptomatischer nicht-anhaltender ventrikulärer Tachykardie (NSVT) identifiziert die programmierte elektrische Stimulation (PES) diejenigen Patient:innen, die von einem ICD profitieren, unabhängig von der NYHA-Klasse [13].
Empfehlung:
- Bei Patient:innen mit KHK, LVEF ≤ 40 % trotz ≥3 Monaten OMT und NSVT (non-sustained ventricular tachycardia) sollte eine ICD-Implantation in Betracht gezogen werden, wenn bei ihnen eine SMVT (sustained monomorphic ventricular tachycardia) durch PES (programmed electrical stimulation) induzierbar ist (Klasse IIa, Level B).
Patient:innen mit dilatativer Kardiomyopathie (DCM)
Eine Metaanalyse aus fünf RCTs mit insgesamt 1854 Patient:innen mit DCM zeigte eine Reduktion der Gesamtmortalität um 31 % durch den Einsatz eines ICDs im Vergleich zur medikamentösen Therapie [14]. Die jüngere DANISH-Studie schloss 1116 symptomatische Patient:innen (NYHA-Klasse II oder III) mit nicht-ischämischer systolischer Herzinsuffizienz (LVEF ≤35 %) ein, die nach OMT randomisiert entweder einen ICD oder keine ICD-Therapie erhielten. Es wurde keine Reduktion des primären Endpunkts der Gesamtmortalität bei Patient:innen beobachtet, die einer ICD-Therapie zugeordnet wurden, obwohl eine signifikante Reduktion des plötzlichen Herztods in der ICD-Gruppe festgestellt wurde [14]. Eine Metaanalyse aller sechs Studien zur Primärprävention zeigte weiterhin eine, wenn auch geringere, Reduktion der Gesamtmortalität durch die ICD-Therapie. Eine Sensitivitätsanalyse zeigte, dass der Nutzen der ICD-Therapie auch nach dem Ausschluss einzelner Studien aus der Metaanalyse bestehen blieb [15].
Empfehlungen:
- Eine ICD-Implantation sollte bei Patient:innen mit DCM, symptomatischer Herzinsuffizienz (NYHA-Klasse II–III) und einer LVEF ≤35% nach ≥3 Monaten OMT in Betracht gezogen werden (Klasse IIa, Level A).
- Eine ICD-Implantation sollte bei DCM-Patient:innen mit einer pathogenen Mutation im LMNA-Gen in Betracht gezogen werden, wenn das geschätzte 5-Jahres-Risiko einer lebensbedrohlichen ventrikulären Arrhythmie ≥10 % beträgt und NSVT, eine LVEF <50 % oder AV-Überleitungsstörungen bestehen (Klasse IIa, Level B).
- Eine ICD-Implantation sollte bei DCM-Patient:innen mit einer LVEF von 50 % und ≥2 Risikofaktoren (Synkope, LGE auf CMR, induzierbare SMVT bei PES, pathogene Mutationen in den Genen LMNA, d PLN, FLNC und RBM20) in Betracht gezogen werden (Klasse IIa, Level C).
Sekundärprophylaxe
Die Sekundärprophylaxe bezieht sich auf die Therapie nach überlebtem Kammerflimmern (VF), das nicht durch reversible Ursachen erklärbar ist, sowie nach ventrikulären Tachykardien (VT) mit symptomatischen oder hämodynamisch relevanten Episoden trotz optimaler medikamentöser Therapie.
Empfehlung:
- Die ICD-Implantation wird bei Patient:innen mit dokumentiertem Kammerflimmern oder hämodynamisch nicht tolerierter ventrikulärer Tachykardie ohne reversible Ursachen empfohlen (Klasse I, Level A).
Patient:innen mit koronarer Herzkrankheit
Eine Metaanalyse zur Sekundärprävention zeigte eine Reduktion der Gesamtmortalität um 28 %, die fast ausschließlich auf eine Verringerung der arrhythmischen Todesfälle in der ICD-Gruppe zurückzuführen war [1].
Empfehlungen:
- Die ICD-Implantation wird bei Patient:innen ohne anhaltende Ischämie mit dokumentiertem Kammerflimmern oder hämodynamisch nicht tolerierter ventrikulärer Tachykardie empfohlen, die später als 48 Stunden nach dem Herzinfarkt auftritt (Klasse I, Level A).
- Bei Patient:innen mit hämodynamisch tolerierter SMVT und einer LVEF von ≥40 % sollte eine ICD-Implantation in Betracht gezogen werden, wenn eine VT-Ablation fehlschlägt, nicht verfügbar ist oder nicht gewünscht wird (Klasse IIa, Level C).
- Bei Patient:innen mit KHK, die für eine ICD-Implantation in Frage kommen, kann eine Katheterablation unmittelbar vor (oder unmittelbar nach) der ICD-Implantation in Betracht gezogen werden, um nachfolgende VT-Belastungen und ICD-Schockabgaben zu verringern (Klasse IIb, Level B).
Patient:innen mit dilatativer Kardiomyopathie
Bei Patient:innen mit DCM zeigte sich ein ähnlicher, jedoch nicht signifikant ausgeprägter Trend zur Reduktion der Mortalität [1]. Trotz fehlender Daten teilen Experten die Auffassung, dass auch bei DCM-Patient:innen mit hämodynamisch tolerierter VT eine ICD-Implantation erwogen werden sollte.
Empfehlungen:
- Die ICD-Implantation wird bei Patient:innen mit DCM empfohlen, die einen SCA aufgrund von VT/VF überleben oder eine hämodynamisch nicht tolerierte SMVT erleiden (Klasse I, Level B).
- Bei Patient:innen mit DCM und hämodynamisch tolerierter SMVT sollte eine ICD-Implantation in Betracht gezogen werden (Klasse IIa, Level C).
Implantation
Prinzipiell unterscheidet sich das Implantieren von Defibrillatorsonden technisch nicht von den Schrittmachersonden. Ein Zugang über die Vena cephalica ist einem über die Vena subclavia vorzuziehen. Um eine sichere rechtsventrikuläre Stimulationsoption zu erhalten, wird zunächst die RV- vor der RA-Sonde implantiert. Die LV-Sondenimplantation kann zuletzt erfolgen, um eine Dislokation der passiv fixierten LV-Sonde durch anschließende Manipulation zu vermeiden.
Der Vergleich zwischen einer septalen und apikalen Platzierung der RV-Sonde gewinnt funktionell an Bedeutung je größer der ventrikuläre Stimulationsanteil ist. Um ein asynchrones Kontraktionsmuster bei einer eingeschränkten Pumpfunktion und somit einer möglichen stimulationsinduzierten progredienten Herzinsuffizienz entgegenzuwirken, kann die Platzierung der rechtsventrikulären Elektrode am mittleren Ventrikelseptum empfehlenswert sein. Hinsichtlich der perioperativen Komplikationsraten zeigte die septale Implantation Vorteile gegenüber der Implantation im Apex oder an der freien Wand [16]. Keinen Unterschied zeigte hingegen der Implantationsort in Bezug auf ineffektive oder unerwünschte Schockabgaben [17,18]. Diesen Daten folgend, sollten auch Defibrillationssonden septal implantiert werden.
Programmierung
Eine gute Wahrnehmung zur Detektion ventrikulärer Arrhythmien ist die grundlegende Voraussetzung von ICD-Systemen für eine sichere Funktion der programmierten ICD-Behandlungsalgorithmen. So kann einerseits ein Undersensing der Kammersignale zum Ausbleiben einer notwendigen Therapieabgabe führen, während andererseits ein fehlerhaftes Oversensing z. B. von T-Wellen zur unerwünschten Schockabgabe führen kann. Dies stellt ein grundlegendes Problem der ICD-Therapie darstellt. Daher sollten regelmäßige ICD-Kontrollen zur Kontrolle der Sondenparameter und zur Optimierung der Programmierung erfolgen bzw. nach jeder dokumentierten Therapie eine kritische Re-Evaluation von Indikation und Programmierung durchgeführt werden, um unnötige Therapieabgaben zu reduzieren (Klasse I, Level A).
Detektionsalgorithmen
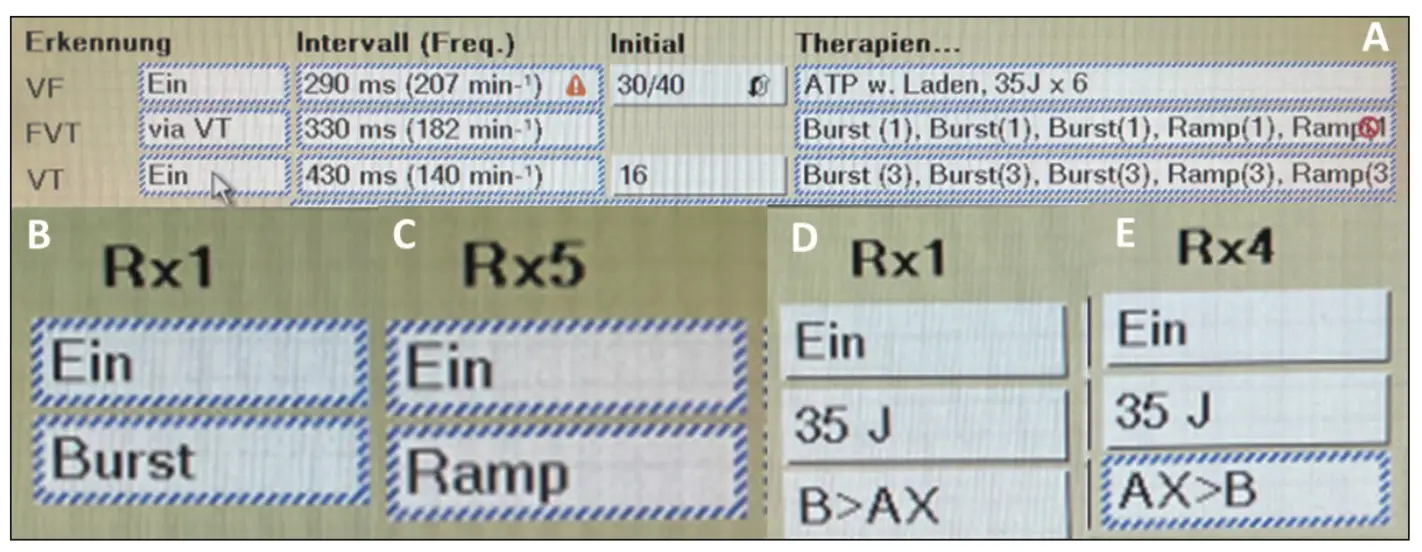
Die Detektionsfunktion von ICDs basiert auf dem Messen der Länge von R-R-Intervallen. Unterschreitet die Dauer des R-R-Intervalls die in 3 unterschiedlichen Detektionszonen (1: VT (ventrikuläre Tachykardie)-Zone; 2: FVT („fast“ VT); VF (ventrikuläres Flimmern)) programmierte Dauer, startet ein Behandlungsalgorithmus. Für jede Zone kann die Form des Algorithmus manuell gewählt werden. Zur Auswahl stehen hier die antitachykarde Therapie (ATP), die Kardioversion und die Defibrillation (Abb. 2).
Einstellungen
- Eine Detektionszone:
Wenn in der Diagnostik ausschließlich Kammerflimmern dokumentiert wurde, reicht die Programmierung nur einer Detektionszone. Da ein gewisses Maß an Undersensing einkalkuliert wird (zur Oversensingprävention), startet die Therapie erst nach Erfüllung einer Sicherheitsmarge aus einer wählbaren Anzahl sicherer R-Zacken in einer wählbaren Phasendauer von wahrgenommenen Signalen (z. B. 70 % oder 30/40) (Abb. 2 A). Detektionszonen sollten mindestens 6–12 s oder 30 Intervalle lang sein (Klasse I, Level A).
- Zwei Detektionszonen:
Wenn das Problem vornehmlich VTs sind, sollten zwei Detektionszonen programmiert werden – eine VT-Zone und eine VF-Zone. Allerdings wird empfohlen, immer mehr als eine VT-Zone zu programmieren (Klasse IIa, Level B).
- Drei Detektionszonen:
Im Falle unterschiedlich schneller VTs in der Diagnostik kann die Programmierung von drei Detektionszonen sinnvoll sein. So ist z. B. eine Slow-VT-Zone zur ausschließlichen ATP-Therapie und eine schnellere VT-Zone programmierbar, die entweder/oder eine andere ATP-Strategie verfolgt oder in der Therapieeskalation zu einem späteren Zeitpunkt erst schockt. Zur effektiven VT- und SVT- Diskrimination sollte eine Zone bis zu einer Frequenz von 230 Schlägen pro Minute gewählt wer- den (Klasse I, Level B).
Antitachykardes Pacing (ATP)
Um Schocktherapien zu vermeiden, lassen sich Kammertachykardien auch durch ein „Überpacen“, eine antitachykarde Stimulation, beenden. Zur ATP-Therapie stehen zwei Pacingstrategien zur Verfügung: (1) der Burst (Frequenz konstant) (Abb. 2 B) und (2) der Ramp (ansteigende Frequenz) (Abb. 2 C). Als erste Therapieoption sollte der Burst programmiert wer- den (Klasse I, Level B). Traditionell ist diese Therapieform nur in den VT- und SVT-Zonen verfügbar. In neueren ICD-Generationen lässt sich eine ATP-Sequenz (Burst) bereits vor und während des Ladens der Schockkondensatoren programmieren. Auf diese Weise kann bei erfolgreicher ATP-Therapie die Abgabe eines Schocks vermieden werden. Bei Patient:innen mit struktureller Herzerkrankung sollte immer mindestens eine ATP-Therapie erfolgen (Klasse I, Level A).
Ausblick
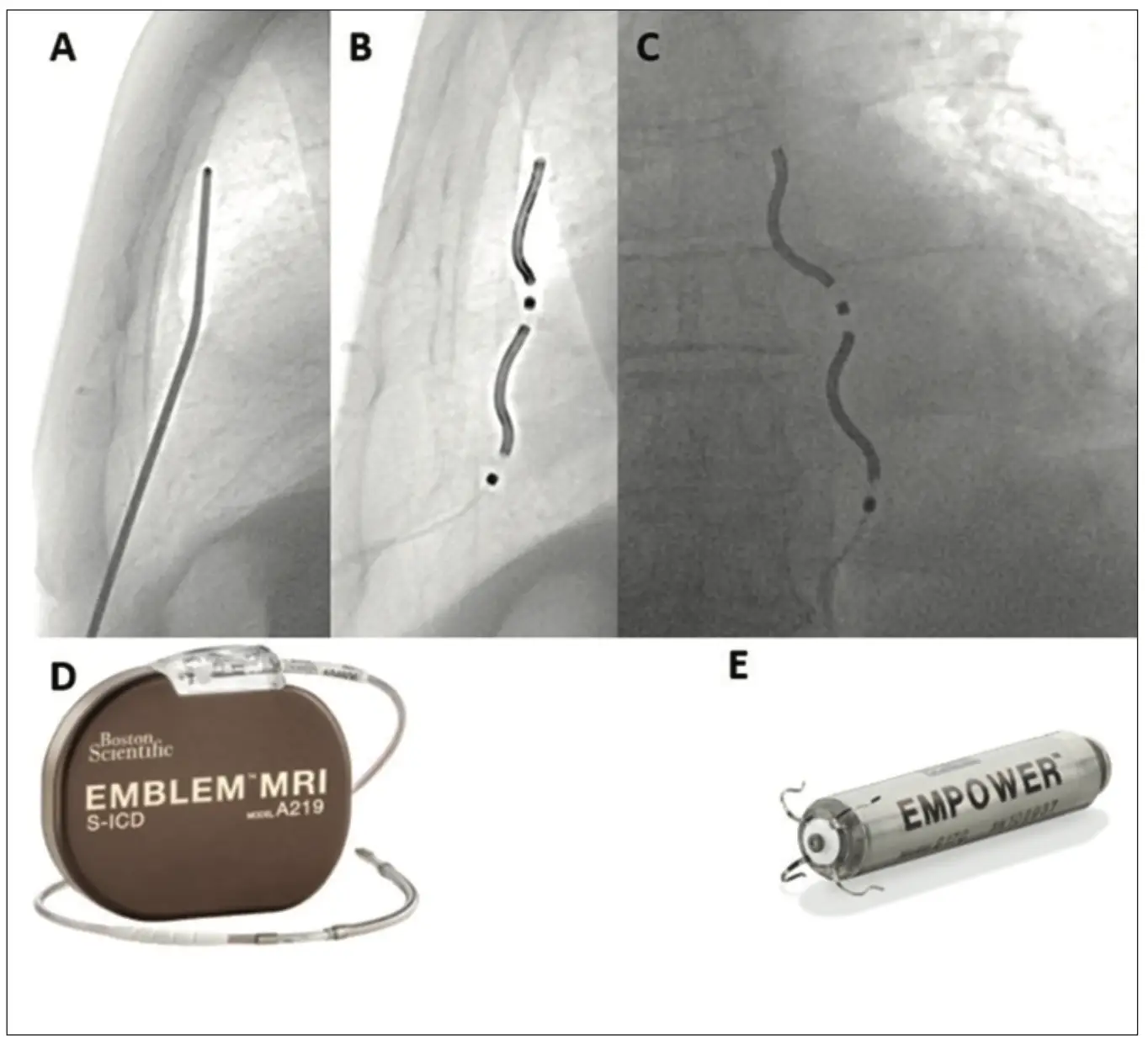
Aktuell drängen neue ICD-Systeme auf den Markt, die eine intravasale Sondenlage vermeiden sollen. Aufbauend auf dem System des „klassischen“ S-ICD (Abb. 1 B) und der prästernalen Elektrodenlage komplettieren Systeme mit einer retrosternalen intrathorakalen Sondenlage das Therapieportfolio durch die Möglichkeit des antitachykarden Pacings. Zudem vermeiden diese Systeme die bekannten Probleme transvenöser Systeme (Infektionen, Sondenbrüche, Gefäßverletzungen, Myokardperforationen, Pneumothoraces, Hämatothoraces und venöse Obstruktionen). Ein extravaskuläres ICD-Modell (Medtronic Aurora EV- ICD) (Abb. 1 D) bedient sich einer substernalen Lage der Schocksonde (Abb. 3 A–C). Funktionsentscheidend ist, dass die Grenzwerte des atrialen (≤0,2 mV) und ventrikulären (≥1 mV) Sensing nicht über- bzw. unterschritten werden sollten, um ein p-Wellen-Over- bzw. R-Zacken-Undersensing zu vermeiden. Innerhalb einer 6-monatigen Follow-up-Periode wurden ventrikuläre Tachykardien zu 50,8 % erfolgreich durch eine ATP-Abgabe terminiert. Induzierte Tachykardien konnten während der Implantation durch eine Defibrillation in 98,7 % der Fälle erfolgreich konvertiert werden. In der gleichen Kohorte kam es allerdings auch bei 29 Patient:innen zu insgesamt 118 unerwünschten Schockabgaben [19].
Ein hybrides extravaskuläres ICD-Modell (Boston Scientific EMBLEM S-ICD, EMPOWER Leadless Pacemaker) (Abb. 3 D+E) besteht zum einen aus einem subkutanen ICD mit prästernaler Schocksonde und einem Leadless-RV-VVI-Schrittmacher. In dieser Kombination mit der extravaskulären Lage der Schockelektrode und dem intrakardialen Herzschrittmacher ergibt sich die zuverlässige Möglichkeit zur Bradykardie-Stimulation und ATP-Abgabe. Bisher finden sich allerdings noch unzureichende klinisch randomisierte prospektive Studien. Die bisherigen Daten zeigen, dass es bei 86 % von 300 Patient:innen innerhalb von 6 Monaten zu keinen schwerwiegenden Komplikationen (Major Complication) kam, was dem vergleichbarer S-ICD-Systeme entspricht [20].
Interessenkonflikt
Die Autoren haben keine finanziellen Interessen oder Beziehungen, die zu Interessenkonflikten führen können.







