Einleitung
Wie schon die erste Episode dieser Reihe, soll auch Teil 2 den Leser:innen eine Hilfe zur Einordnung und Umsetzung der aktuellen Empfehlungen der 2024-EACTS/EACTAIC/ EBCP-Guideline zum kardiopulmonalen Bypass (CPB) in den klinischen Alltag geben. Mittlerweile gehört diese Guideline (GL) zu den meistgelesenen Artikeln im Fachbereich Perfusiologie, Kardiochirurgie und -anästhesie, im renommierten British „Journal of Anaesthesia“ ist sie sogar
der fünft-meistgelesene Artikel 2025 (DOI: 10.1016/j.bja.2025.01.015). Dies zeigt das hohe Interesse an der extrakorporalen Technologie und dem Fachgebiet Perfusiologie.
In diesem Teil werden zwei Kapitel mit 30 Empfehlungen besprochen. Einige der vorgestellten Verfahren sind bereits sehr ausführlich in der Guideline beschrieben, andere wiederum werden in ihrer Anwendung weniger detailliert erklärt. Die Autor:innen der vorliegenden Publikation beschreiben aus diesem Grund manche Verfahren hier genauer, während andere im Text der Originalpublikation nachzulesen sind. Zum besseren Verständnis sollten beide Publikationen komplementär verwendet werden.
Der hier besprochene Teil der GL beschäftigt sich mit dem Monitoring und Sicherheitseinrichtungen der Herz-Lungen-Maschine sowie patientennahen nichtinvasiven und hämodynamischen Überwachungsmöglichkeiten und den Möglichkeiten des Organschutzes während und nach dem kardiopulmonalen Bypass. Das zweite Kapitel beschäftigt sich mit dem Schutz der Organe und enthält sehr viele neue Empfehlungen, während im Kapitel Monitoring nur zwei neue Empfehlungen, jedoch einige Aktualisierungen, hinzugekommen sind.
Mit einem vom European Board of Extracorporeal Perfusion (EBCP) für diese Guideline entwickelten Excel-Tool können die Empfehlungen kompakt und im Abgleich zu 2019 angesehen werden. Weiterhin kann dieses Tool genutzt werden, um die Empfehlungen leichter in die Routine und Standards der Klinik zu übernehmen. Das Tool und die Guideline sind unter folgendem Link auf der Website des EBCP zu finden.
Monitoring
Erweiterte Sensorik und detaillierte Überwachungsmaßnahmen während des CPBs sind integraler Bestandteil einer modernen Perfusionsführung. Eine effektive Überwachung sollte dabei strukturiert, multimodal und risikoadaptiert erfolgen, mit klar definierten Zielbereichen für Perfusion, Organfunktion und Hämodynamik.
Über prädiktive Messungen können einerseits unerwünschte Zwischenfälle, wie zum Beispiel das Versagen des Oxygenators durch die Delta P-Messungen, besser vorhergesagt oder vermieden werden. Anderseits werden aber auch Minder- oder Malperfusionen schneller erkannt, insbesondere dann, wenn patientennahe Parameter überwacht werden. In der GL 2024 zeigt sich ein eindeutiger Trend zu mehr Empfehlungen, welche sich auf direkte und patientennahe Überwachung beziehen. So sind Empfehlungen zur Neuro- und der erweiterten hämodynamischen Überwachung neu hinzugekommen.
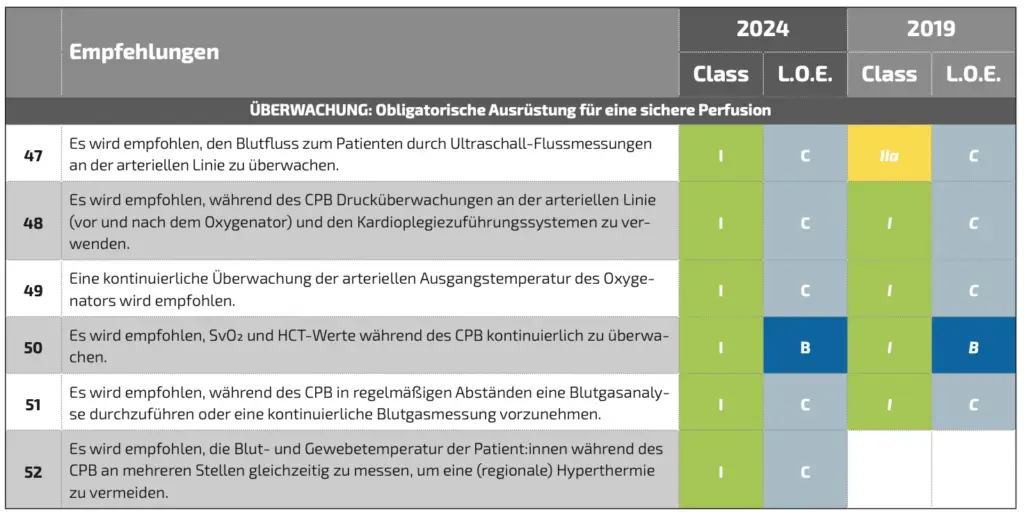
Obligatorische Überwachungen für eine sichere Perfusion
Als wichtige Basisgrößen für physiologische Patientenpara-meter gelten nach wie vor die Druckmessungen, die Pumpenflüsse und regelmäßige Blutgasanalysen (I C). Auch werden weiterhin der Messung der venösen Sauerstoffsättigung und der kontinuierlichen Blutgasüberwachung eine erhebliche Bedeutung zugesprochen (I B).
Bezüglich der zu überwachenden Temperaturen werden neben der Messung der arteriellen Auslasstemperatur des Oxygenators nun auch multiple Blut-/und Gewebemessungen empfohlen, um lokale Hyperthermien zu vermeiden (Neu: I C). Bei der Anwendung von Rollenpumpen als arterielle Pumpe wird traditionell oft noch ein rein berechneter Fluss als Wert aus den Umdrehungen verwendet. Dies birgt ein hohes Risiko für falsche Werte, auf die sich dann wiederum die gesamte Perfusionsführung wie die Berechnungen zum Sauerstofftransfer (Goal directed perfusion), aber auch die Gabe von vasoaktiven Medikamenten bezieht. Dieses Risiko lässt sich mit einer Echtzeitmessung des arteriellen Pumpenflusses mittels Ultraschalls deutlich minimieren, der Empfehlungsgrad hierfür wurde von IIa C auf I C erhöht. Es wird außerdem empfohlen, dass der Fluss möglichst patientennah (nach allen Shunts des CPB) gemessen werden soll, um korrekte Messwerte zu gewährleisten.
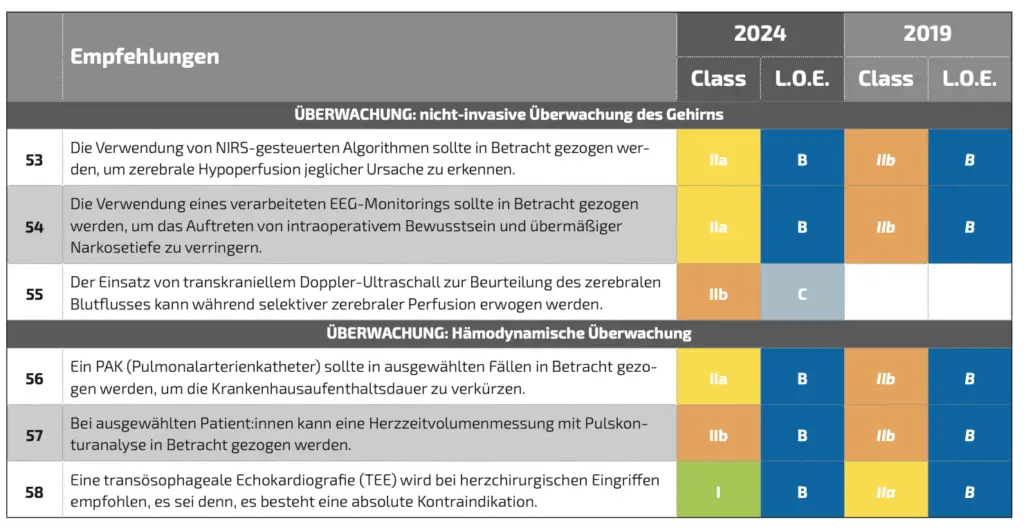
Nicht-invasive Überwachungen des Gehirns
Die Leitlinie empfiehlt das kontinuierliche Monitoring der regionalen zerebralen Sauerstoffsättigung (rScO₂) mittels Nahinfrarote Regionale Spektroskopie (NIRS), um eine zerebrale Desaturation frühzeitig zu erkennen und die Perfusionsparameter gezielt anpassen zu können. Hierbei wird der Einsatz der NIRS-Messung, insbesondere bei Hochrisikopatient:innen und komplexen Eingriffen, nahegelegt. Sie kann aber auch bei dem Routine-CPB als Bestandteil eines erweiterten Monitorings dienen. Die Empfehlungsgrade für die nahinfrarote Spektroskopie zur Beurteilung der regionalen Sauerstoffversorgung des Hirngewebes und die Elektroenzephalogramm-(EEG)-basierte Überwachung der Narkosetiefe wurden bei einer jeweiligen Literaturstärke von B von IIb auf IIa erhöht.
Das Monitoring der Narkosetiefe (Depth of Anaesthesia, DOA) wird zur Reduktion von Awareness-Risiko und zur Optimierung der Anästhesiedosierung während der Herzoperation mit CPB besonders empfohlen. Die Leitlinie argumentiert die Erhöhung des Empfehlungsgrades von IIb B auf IIa B damit, dass die „intraoperative Awareness“ bei kardiochirurgischen Patient:innen häufiger auftritt als in der Nicht-Herzchirurgie, weshalb ein strukturiertes DOA-Monitoring hier besonders relevant ist.
Der Einsatz der transkraniellen Dopplersonographie (TCD) (Neu: IIb C) wurde der Leitlinie neu hinzugefügt und gilt als ergänzendes Verfahren des Neuromonitorings zur Embolie- und Perfusionsüberwachung während des CPB. Die Leitlinie hebt hervor, dass der TCD die Embolielast, Perfusionsmuster und mögliche Seitenunterschiede sichtbar machen kann, der direkte Einfluss auf harte klinische Endpunkte (z. B. Schlaganfall, Neurokognition) aber bislang limitiert und heterogen belegt ist. Empfohlen ist der TCD vor allem bei Hochrisikoeingriffen (z. B. Aorten-/Aortenbogenchirurgie) und in Zentren mit entsprechender Expertise und Ressourcen. Auch sind die Einsatzmöglichkeiten eingeschränkt, da für die Anwendung geschultes Personal, geeignete Akustikfenster (meist A. cerebri media) und standardisierte Protokolle zur Interpretation von Emboliesignalen und Flussveränderungen erforderlich sind.
Hämodynamische Überwachung
Dieser Abschnitt beschreibt die hämodynamische Überwachung während des CPB und fordert ein strukturiertes, multimodales Monitoring von Druck, Volumen, Herzfunktion und Organperfusion über das reine EKG hinaus. Ziel ist eine individualisierte Steuerung von Pumpfluss und Blutdruck, um Organdysfunktionen und Komplikationen zu minimieren.
Pulmonalarterienkatheter (PAK)
Obwohl der Pulmonalarterienkatheter (PAK) nicht routinemäßig bei allen CPBs eingesetzt werden soll, wird sein Stellenwert als invasives erweitertes hämodynamisches Monitoringinstrument in ausgewählten Hochrisikosituationen als sinnvoll anerkannt und der Empfehlungsgrad hat sich für die-se Patientengruppe von IIb B auf IIa B erhöht.
Minimalinvasive hämodynamische Monitore
Minimalinvasive hämodynamische Monitore können auf Basis der Pulskonturanalyse als Alternative bzw. Ergänzung zum Pulmonalarterienkatheter zur Steuerung von Volumen- und Kreislauftherapie verwendet werden. Da die Anwendung jedoch methodisch eingeschränkt ist (z. B. unter CPB, bei Arrhythmien, stark veränderter vaskulärer Compliance, offenen Thoraxbedingungen, niedrigen Tidalvolumina) und somit die Genauigkeit reduziert sein kann, bleibt auch der Empfehlungsgrad mit IIb B vergleichsweise niedrig.
Transösophageale Echokardiographie (TEE/TOE)
Die transösophageale Echokardiographie (TEE/TOE) erhält in der Guideline eine Erhöhung von IIa B auf I B. Sie gilt laut Guideline als zentrales erweitertes hämodynamisches Monitoring- und Diagnostiktool in der Herzchirurgie, das in vielen Zentren faktisch zum Standard gehört. Die Evidenzbasis sowie die Verfügbarkeit des TEEs hat seit der letzten GL klar zugenommen. Seit 2019 liegen mehr Daten vor, so dass durch ein TEE relevante Befunde entdeckt werden können (z. B. residuelle Klappenfehler, Thromben, LV/RV-Dysfunktion, Aortenerkrankungen), die unmittelbar zu Therapieänderungen führen, Therapieanpassungen, aber auch Re-Operationen und hämodynamische Instabilität verhindern können. Die 2024-Leitlinie beschreibt TEE ausdrücklich als integralen Bestandteil des hämodynamischen Monitorings und nicht nur als „zusätzliches“ Verfahren und hebt dabei besonders seinen Nutzen beim Weaning von dem CPB und der Ursachensuche bei hämodynamischer Instabilität hervor.
Organprotektion
Dieses Kapitel behandelt den Themenkomplex Organprotektion während der Herzoperation mit CPB. Er bündelt die Evidenz zu Strategien, mit denen Herz, Gehirn, Niere, Lunge und andere Organe vor CPB-assoziierter Ischämie-Reperfusion, Entzündung und Embolie geschützt werden sollen. Zu diesen Maßnahmen gehören die Remote Ischaemic Preconditioning oder auch induzierte ischämische Präkonditionierung, pharmakologische Maßnahmen wie Statine oder beta-adrenerge Blocker sowie organspezifische Maßnahmen in Bezug auf Gehirn, Herz, Nieren und Lunge.
Remote Ischaemic Preconditioning
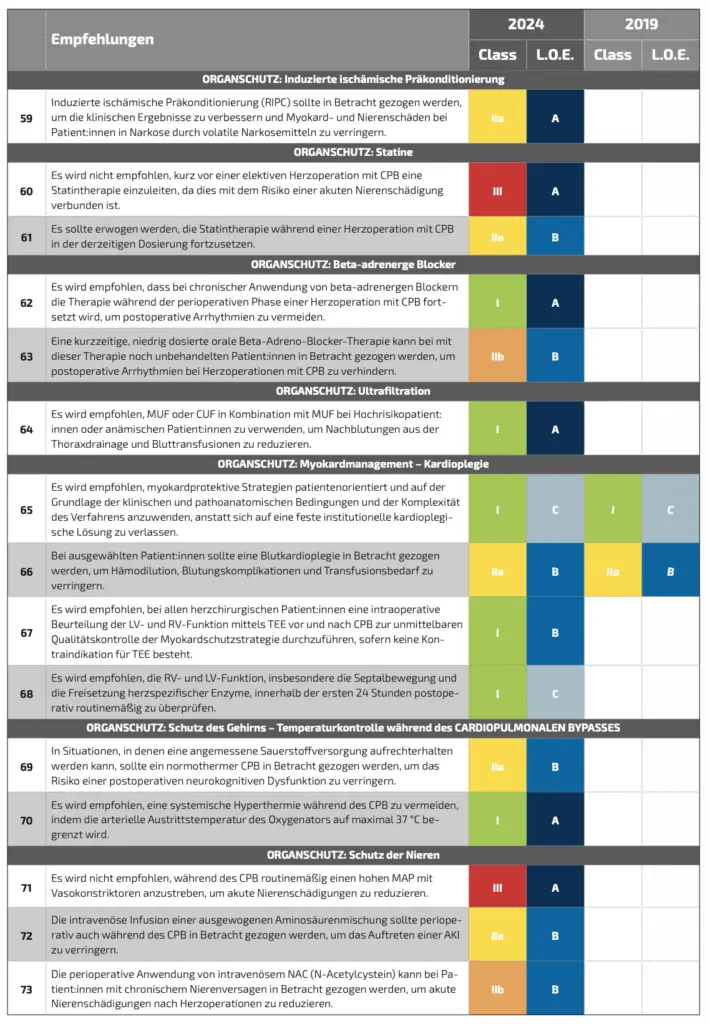
Beim Verfahren der Remote Ischaemic Preconditioning (RIPC) wird eine wiederholte kurzzeitige Ischämie eines peripheren Gewebes (meist Arm oder Bein) mittels Blutdruckmanschette erzeugt, um das Myokard und andere Organe vor Ischämie-Reperfusionsschäden während des CPB zu konditionieren und damit zu schützen. Die Leitlinie bewertet RIPC als praktisches, kostengünstiges und weitgehend risikofreies Zusatzverfahren mit gemischter, aber vielversprechender Evidenz und empfiehlt (IIa A) sie optional als Bestandteil eines umfassenden Organprotektion-Konzepts, dies allerdings nicht als verpflichtenden Standard.
Dies gilt zurzeit allerdings nur für Patient:innen unter Narkose mit volatilen Anästhetika, da neuere Metaanalysen zeigen konnten, dass Propofol und andere Narkosemedikamente einen deutlichen Einfluss auf die Ergebnisse der ischämischen Präkonditionierung haben können [DOI: 10.1093/ndt/gfx210]. Zu den weiteren unklaren Störfaktoren gehören Medikamente wie Nitrate und Sulfonylharnstoffe und unterschiedliche Anästhesieprotokolle. Somit, so argumentieren die GL-Autor:innen, könnte sich die Variabilität in den Studienergebnissen zumindest teilweise erklären.
Statine
Der Einsatz von Statinen als pharmakologische Organprotektion im Kontext der Herzchirurgie mit CPB, vor allem mit Blick auf kardiovaskuläre und entzündungsmodulierende Effekte, wird durch die Leitlinie anerkannt. Eine bereits bestehende Medikation (Beginn mind. 30 Tage vor OP) mit Statinen sollte (IIa B) daher perioperativ fortgesetzt werden.
Allerdings wird die kurzfristige Einnahme direkt vor der OP nicht empfohlen (III A), da die aktuelle Studienlage, die zunächst vermuteten Vorteile nicht bestätigen konnte (DOI: 10.1056/NEJMoa1507750) und es zudem in einigen Studien sogar zu einem erhöhten Auftreten von postoperativem Nierenversagen kam, wenn Statine kurzfristig vor der Operation eingenommen wurden (DOI: 10.1001/jama.2016.0548).
Beta-Blocker
Dieser Abschnitt behandelt den Einsatz von Beta-Blockern im perioperativen Setting der Herzchirurgie mit CPB als Bestandteil der Organprotektion, insbesondere zum Schutz des Myokards und zur Rhythmuskontrolle. Beta-Blocker werden mit einem geringeren Risiko für perioperative Myokardischämien und Arrhythmien (insbesondere Vorhofflimmern) in Verbindung gebracht und gelten daher als etablierter Be-standteil der kardiovaskulären Dauermedikation.
Viele Patient:innen kommen bereits mit einer chronischen Betablocker-Therapie zur Operation; sofern keine Kontraindikationen (z. B. schwerer Schock, relevante Bradykardie) vorliegen, wird empfohlen, die Therapie perioperativ fortzuführen (I A).
Die Leitlinie sieht dabei einen Nutzen v. a. in der Prävention postoperativer Vorhofflimmerepisoden und in einer Reduktion der myokardialen Belastung, betont aber, dass Dosierung und Zeitpunkt individuell und in Abhängigkeit von der Hämodynamik gewählt werden müssen.
Ein routinemäßiger Neu-Beginn mit hochdosierter Betablocker-Gabe als ausschließliche „CPB-Organprotektion“ wird nicht gefordert, kann aber erwogen werden (IIb B), entscheidend ist vielmehr die sinnvolle Fortführung/Anpassung der bestehenden Therapie im Rahmen eines ganzheitlichen perioperativen Konzepts.
Ultrafiltration (Hämofilter)
Die Ultrafiltration ist eine Technik, die während des CPB zum Volumenmanagement und/oder zur Reduzierung schädlicher Bestandteile eingesetzt wird. Die am häufigsten verwendeten Techniken sind die konventionelle Ultrafiltration (CUF), die Null-ausgeglichene Ultrafiltration (ZBUF) und die modifizierte Ultrafiltration (MUF). Die modifizierte Ultrafiltration (MUF) wird als Technik beschrieben, bei der nach Beendigung des CPB über einen separaten Kreislauf Ultrafiltrat entfernt wird, um die Hämodilution durch das HLM-Restblut zu reduzieren. Somit können unter Erhalt der Proteine und Elektrolyte der Hämoglobin-/Hämatokritwert erhöht und potenziell auch Entzündungsmediatoren entfernt werden.
Die Leitlinie sieht potenzielle Vorteile für die Regulierung des Volumenstatus, der Lungenfunktion und ggf. einer Reduktion der Blutungsneigung, weist aber auf eine begrenzte und heterogene Evidenz im Erwachsenenkollektiv hin und empfiehlt MUF (I A) als optionale Technik, nicht jedoch als Standard für alle Patient:innen.
Myokardmanagement – Kardioplegie
Dieser Abschnitt behandelt das myokardiale Management mittels Kardioplegie und fasst Empfehlungen zu Auswahl, Dosierung und Anwendung von Kardioplegielösungen während des CPB zusammen. Es werden verschiedene Konzepte (z. B. kristalloide vs. Blutkardioplegie, antegrade vs. retrograde Applikation, intermittierende vs. kontinuierliche Gabe, Temperaturregime) beschrieben und hinsichtlich Evidenz und Praktikabilität verglichen. Adressiert werden zudem Qualitätskriterien der Myokardprotektion (z. B. Druck, Volumen, Intervalle der Re-Dosis, Monitoring von Temperatur und Rhythmus), dabei wird besonders auf die hohe Bedeutung standardisierter, protokollbasierter Vorgehensweisen hingewiesen.
Ziel jeder Form von Kardioplegie ist die Myokardprotektion, also ein möglichst vollständiger, aber reversibler Herzstillstand mit optimalem Schutz vor Ischämie-Reperfusionsschäden im Rahmen der Aortenklemmung. Die Leitlinie betont, dass nicht eine einzelne „ideale Kardioplegiestrategie“ existiert, sondern dass das Verfahren an den Patient:innen, den Eingriff und die Zentrumserfahrung angepasst werden sollen. Im Text der Leitlinie werden die Prinzipien der Kardioplegie, sowohl klassische als auch moderne Kardiolegieverfahren, ausführlich beschrieben. Zudem findet sich ein Abschnitt zur Diagnostizierung von post-ischämisch geschwächtem Myokard (myocardial stunning) durch suboptimalen Myokardschutz.
Für die Leitlinie gehören zum Myokardmanagement auch die Kontrolle der myokardialen Funktion. Somit sind zwei Empfehlungen in der 2024er Version hinzugekommen: Mit Grad I wird empfohlen, bei allen Patient:innen, ohne Kontraindikation zum transösophageale Echo (TEE) sowohl intraoperativ (I B) als auch postoperativ (I C) ein TEE durchzuführen.
Für Patient:innen mit niedriger Körperoberfläche und/oder Neigungen zu Blutungen sollte eine Blutkardioplegie in Betracht gezogen werden, um die Hämodilution, Blutungskomplikationen und den Transfusionsbedarf zu reduzieren (IIa B).
Zerebrale Protektion durch Temperaturkontrolle während des CPB
Hier wird die zerebrale Protektion durch Temperaturkontrolle während des CPB beschrieben. Im Zentrum des Textes stehen Empfehlungen zu Hypo-/Normothermie, Messung und Wiedererwärmung, um neurologische Schäden zu vermeiden.
In der Leitlinie werden die Rollen von Hypo- und Normothermie diskutiert und kritisch bewertet. Die physiologischen Auswirkungen der Hypothermie insbesondere auf die cerebrale Toleranz bei inadäquater Versorgung mit Sauerstoff (reduzierter DO2) lassen die Autor:innen unbestritten, dennoch weisen sie auch auf die Risiken wie einen möglichen neuronalen Zelluntergang, Koagulopathie und Hyperthermie während der Aufwärmphase hin. Hier ist die Empfehlung mit I A sehr klar nicht über 37 °C Austrittstemperatur am Oxgenator zu wärmen.
Für Routineeingriffe wird somit eher eine milde Hypothermie oder Normothermie empfohlen (IIa B), während die tiefe Hypothermie speziellen Indikationen (z. B. komplexe Aortenbogenchirurgie) vorbehalten bleibt.
Zudem wird ein standardisiertes Temperaturmanagement mit multiplen Kern- und peripheren Messstellen (z. B. nasopharyngeal, Ösophagus, Blase) gefordert, um reale zerebrale Temperaturen besser abzubilden.
Die Leitlinie empfiehlt, Temperaturgradienten zwischen Oxygenator-Auslass und venösem Rücklauf sowie die Aufwärmgeschwindigkeit zu begrenzen (angelehnt an STS/SCA-Empfehlungen), um Gasblasenbildung und zerebrale Hyperthermie zu verhindern.
Nierenschutz
Der Abschnitt fasst Strategien zusammen, die über eine reine Modifikation von CPB-Techniken, Temperatur oder Kardiopleie hinausgehen und direkt auf zelluläre Mechanismen von Ischämie-Reperfusion, Entzündung und oxidativem Stress abzielen.
Das akute Nierenversagen (AKI) tritt bei 5–40 % der kardiochirurgischen Patient:innen auf, ist mit erhöhter Morbidität, Mortalität und einem anhaltenden Risiko für chronische Nierenerkrankungen (CKD) assoziiert und wird durch multiple perioperative Noxen einschließlich der extrakorporalen Zirkulation verursacht.
Blutdruck
Die GL diskutiert intensiv die Vor- und Nachteile der Führung der Perfusion bezüglich des mittleren arteriellen Blutdrucks
(MAP). Sie kommt dabei zu dem Schluss, dass ein hoher Blutdruckzielwert (je nach Studie MAP > 60 bis MAP > 80) nur geringe bis gar keine Auswirkungen auf die Patientenergebnisse, einschließlich AKI und Todesfälle, haben kann. Es ist den Autor:innen wichtiger, einen normalen DO2 anzustreben, den Blutfluss des CPB zu optimieren und Marker der Gewebeperfusion (NIRS und SvcO2) zu überwachen und normalwertig zu halten, als Vasopressoren zur Erhöhung des MAP einzusetzen (III A).
Aminosäuren zur Nierenprotektion
Hier wird die intravenöse Gabe von Aminosäuren zur Nierenprotektion während des CPB beschrieben. Begründet wird die Intervention mit potenziell renoprotektiven Effekten durch eine verbesserte renale Durchblutung, osmotische Diurese und Unterstützung des Stoffwechsels der Niere im Stresszustand. Allerdings ist die Evidenzlage gering, es werden wenige, überwiegend kleine Studien beschrieben, in denen parenterale Aminosäuren perioperativ bzw. intraoperativ gegeben wurden, um akute Nierenschäden (AKI) nach Herzoperationen zu reduzieren. Dennoch empfehlen die Autor:innen der GL die Therapie mit einem Grad von IIa B.
Gabe von N-Acetylcystein zur Nierenprotektion
N-Acetylcystein wirkt an der Niere vor allem über antioxidative und vasodilatatorische Effekte, die Tubuluszellen vor Schäden schützen und die renale Durchblutung (Mikrozirkulation) verbessern sollen (PMCID: PMC8129408 PMID: 34017406). NAC wirkt dabei über die Erhöhung der NO-Verfügbarkeit und Modulation von Vasokonstriktoren (DOI: 10.34172/ npj.2023.11658).
Allerdings kommen die Autor:innen der GL zu dem Schluss, dass N-Acetylcystein (NAC) zur Nierenprotektion bei herzchirurgischen Patient:innen unter CPB nicht höher als mit IIb B empfohlen werden kann, da der vorhandene Evidenzkörper keinen klinisch relevanten Nutzen zeigt. Ein klinischer Nutzen tritt nur dann ein, wenn das Medikament intravenös mit adäquater hoher Dosierung gegeben wird.
Strategien zum Lungenschutz während des CPB
In diesem Kapitel werden Strategien zum Lungenschutz während und nach CPB beschrieben, die Verfahren sind die selektive pulmonal arterielle Perfusion, verschiedene Ventilationsformen während des CPB und Steroide zum Schutz der Lunge.
Selektive Pulmonalarterien-Perfusion
Die selektive Pulmonalarterien-Perfusion während des CPB bedeutet, dass die Lunge trotz aortaler Klemmung gezielt weiter durchströmt wird, um den Ischämie-Reperfusionsschaden zu begrenzen. Bei dem Verfahren wird die Lunge während des CPB gezielt mit einem niedrigen, kontrollierten Fluss weiter perfundiert, meist mit oxygeniertem Blut oder gelegentlich mit HTK-Lösung. Ziel ist es, die klassische CPB-bedingte „Lungenstilllegung“ (Hypoperfusion und Kollaps) zu vermeiden und so Ischämie-Reperfusionsschäden, endotheliale Dysfunktion und inflammatorische Aktivierung im Lungengewebe zu reduzieren (doi: 10.1002/14651858. CD011098.pub2).
Die Leitlinie beschreibt, dass kleinere Single-Center-RCTs zeigen, dass insbesondere die pulsatile Perfusion der Pulmonalarterie mit oxygeniertem Blut biochemische Zeichen von Lungenschäden reduzieren kann und sich teilweise die Oxygenierung verbessert, jedoch ohne klaren klinischen Benefit bei harten Endpunkten. Auch eine zitierte Cochrane-Analyse stuft die Evidenzqualität als sehr niedrig ein; Effekte auf Mortalität, schwere Nebenwirkungen und PaO₂/FiO₂-Ratio bleiben unsicher, weshalb der Nutzen insgesamt als nicht belegt gilt. Konsequenterweise ist der Empfehlungsgrad niedrig, allerdings und insbesondere bei hohem pulmonalem Risiko kann selektive pulmonale Perfusion erwogen werden (IIb B).
Ventilationstechniken während des CPB
Zu den verschiedenen Möglichkeiten von Ventilationstechniken gehören die fortgesetzte Anwendung von Continuous Positive Airway Pressure (CPAP), Vital-Capacity-Manöver und niedrigvolumige Ventilation während CPB. Diese Verfahren sollen konsistent die frühe postoperative Oxygenierung verbessern.
Bei CPAP bleiben die Patient:innen während des CPB kontrolliert beatmet (offen ventilierte Lunge), typischerweise mit einem kontinuierlichen, positiven Atemwegsdruck (z. B. 5–10 cm H₂O) ohne oder mit minimalem Atemzugvolumen (doi: 10.1213/ ANE.0000000000001118).
Das Verfahren soll dabei die alveolären Strukturen stabilisieren, ein zyklisches Kollabieren/Re-Recruitment reduzieren, die funktionelle Residualkapazität und das V/Q-Verhältnis verbessern und so frühe postoperative Atelektasen und Shuntbildung verringern.
Bei der sogenannten „Low-Tidal-Volume-Ventilation“ wird die Lunge während des CPB mit sehr niedrigen Tidalvolumina (z. B. 3 ml/kg, ca. 5 Atemzüge/min) plus PEEP (ca. 5 cm H₂O) kontinuierlich mechanisch ventiliert. Diese protektive Ventilation kombiniert PEEP-vermittelte Alveolarstabilisierung mit minimaler zyklischer Dehnung, um eine Volutrauma- und Atelektasetrauma-bedingte Inflammation zu vermindern, gleichzeitig aber den Gasaustausch und Surfactant-Funktion zu erhalten (doi: 10.1213/ANE.0000000000001118).
Das Verfahren des „Vital-Capacity-Manövers (VCM)“ bedeutet, dass kurzzeitige Rekrutierungsmanöver mit hohen inspiratorischen Drücken (z. B. 30–40 cm H₂O für einige Sekunden), die intermittierend während des CPB oder unmittelbar vor Weaning durchgeführt werden, einhergehen (doi.org/10.3389/ fcvm.2016.00047). Dabei sollen die Manöver kollabierte Alveolen schlagartig öffnen, Atelektasen reduzieren und somit kurzfristig die Compliance und den PaO₂/FiO₂-Quotienten verbessern. Dabei kann es aber auch zu hohen Drücken und zu einem Barotrauma oder hämodynamischer Beeinträchtigung kommen.
Obwohl die vorgestellten Ventilationstechniken eine Verbesserung im Vergleich zu einer vollständig „stillgelegten“ Lunge zeigen, finden sich in Meta-Analysen und größeren RCTs jedoch bislang keine klaren Vorteile bei harten Endpunkten wie Mortalität, Beatmungsdauer oder ARDS-Inzidenz. Die Techniken werden daher zwar primär als physiologisch plausibel und sicher, aber mit begrenztem nachgewiesenem Outcome-Benefit eingestuft. Sie werden aus diesem Grund in der Leitlinie nicht empfohlen (III A).
Steroide
Der CPB triggert über Blut–Fremdoberflächenkontakt, Ischämie-Reperfusion und Endothelaktivierung eine SIRS-artige Antwort mit Freisetzung von TNF-α, IL-6, IL-8, Komplementaktivierung und Endothelschaden, was zu Hypotonie, Myokarddepression und pulmonalem Gasaustauschdefizit führen kann (https://doi.org/10.1378/chest.112.3.676). Steroide werden im Kontext vom CPB gegeben, sie sollen die überschießende systemische Inflammationsreaktion dämpfen und so eine mögliche Organdysfunktion der Lunge begrenzen; ihre Wirkung beruht auf breiter immunmodulatorischer und endothelialer Stabilisierung.
Aufgrund der aktuellen Studienlage kommt die Leitlinie zu dem Schluss, dass die prophylaktische Steroidgabe zur Lungenschutz-Strategie bei CPB zwar die Inflammationsantwort dämpft, aber keinen klaren Nutzen in harten klinischen Endpunkten zeigt und zum Teil sogar die kardialen Risiken erhöhen kann.
Ein möglicher Nutzen könnte für Subgruppen mit hoher vorbestehender inflammatorischer Last bestehen, ist aber bislang nur hypothesengenerierend und rechtfertigt keine routinemäßige Anwendung.
Eine prophylaktische Steroidgabe wird nicht als generelle Standardmaßnahme zur Lungenschutz-Prophylaxe bei CPB empfohlen (III A).
Fazit
Die Kapitel Monitoring und Organprotektion der 2024-EACTS/ EACTAIC/EBCP-Guideline zeigen, dass eine sichere Anwendung des kardiopulmonalen Bypasses nicht primär durch einzelne spektakuläre Interventionen, sondern durch das Zusammenspiel aus strukturiertem Monitoring und organorientierter Protektion erreicht werden kann. Das Monitoring stellt dabei die Voraussetzung für eine individualisierte Steuerung von Blutfluss, MAP, Temperatur und Gastransfer dar, während evidenzbasierte Protektionsstrategien für Herz, Gehirn, Niere und Lunge darauf abzielen, die systemische Ischämie-Reperfusions- und Inflammationslast zu begrenzen. Für die klinische Praxis bedeutet dies, dass Standardmaßnahmen mit hoher Evidenz (z. B. qualitätsgesichertes Basismonitoring, optimierte Hämodynamik, sorgfältige Myokardprotektion, kontrollierte Temperaturführung) konsequent umgesetzt und potenziell protektive, aber schwächer belegte Verfahren (z. B. selektive pulmonale Perfusion, bestimmte Pharmaka) risikoadaptiert und im Kontext der Gesamtevidenz eingesetzt werden sollten.
Biosketch: Dr. Adrian Bauer, PhD, MCT, ECCP
Dr. Adrian Bauer is a clinical perfusionist and Head of the De-partment of Perfusion at the Evangelic Heart Center Coswig, Germany. He holds a PhD in Health Sciences from Aarhus Uni-versity, a Master in Cardiovascular Technology, and the European Certificate in Cardiovascular Perfusion.
After early training as a nurse and perfusionist, Dr. Bauer progressed from Deputy Chief Perfusionist at the University Heart Centre Leipzig to leading the perfusion team at Heart Centre Coswig since 2003. His educational journey includes international qualifications and a strong focus on advancing clinical standards in perfusion.
Dr. Bauer’s research emphasizes minimal invasive extracorporeal circulation (MiECC), blood and transfusion management, coagulation, and perfusion technology innovation. He has authored or co-authored over 20 peer-reviewed publications and book chapters and contributed to key European guidelines and consensus statements on perfusion and cardiac surgery.
He has served in leadership and editorial roles, including President and Vice President of the German Society for Car-diovascular Engineering (DGfK), board member of the European Board of Cardiovascular Perfusion (Vice Chair, EBCP), and editorial boards of major journals. Further, he is a dedicated mentor and lecturer at universities and perfusion schools across Europe.
Dr. Bauer has received several awards recognizing his contributions to minimized extracorporeal circulation and clinical perfusion practices. His professional memberships span national and international societies, reflecting his commitment to innovation, education, and excellence in cardiac surgery and perfusion science.