Einleitung
Die Durchführung des RAP im Rahmen des Einsatzes der Herz-Lungen-Maschine (HLM) ist ein Standardverfahren zur Reduktion der initialen Hämodilution während der Herzoperation. In der Folge kann der intraoperative Fremdblutverbrauch gesenkt oder vermieden werden [2,3,5-14]. In Kombination mit einem gut verzahnten Patient Blood Management (PBM), wie Zacharowsky und Meybohm et al. es in ihren Arbeiten beschreiben, kann der Fremdblutverbrauch während der Therapie deutlich reduziert werden. Dies stellt die Kliniken allerdings in der Praxis vor größere Herausforderungen in der Organisation der prä-, intra- und postoperativen Abläufe [15–26]. Likosky et al. beschreiben in ihrer Arbeit von 2016, dass die Herzchirurgie in den Vereinigten Staaten allein für 15–20 % des Fremdbluteinsatzes im Operationssaal verantwortlich sind [27]. Wir halten es daher als Perfusionisten für geboten, die initiale Hämodilution bei der Etablierung der EKZ so gering wie möglich zu halten. Ein restriktiver Volumeneinsatz, während der EKZ in Verbindung mit einem hypovolämen Beenden der Perfusion und anschließenden „Auffüllen“ des Patienten mit dem verbleibenden Volumen des EKZ-Systems bietet uns die Möglichkeit, Fremdblutgaben zu reduzieren oder ganz zu vermeiden [1,2,7,28]. Der Einsatz des RAP ist eine Klasse 1, Level A-Empfehlung in der CPB-Guideline von 2019 sowie in der PBM-Guideline der EACTS von 2024 [3,4]. Dem Perfusionisten kommt beim Einsatz des Verfahrens die zentrale Rolle zu [27,29]. Trotzdem berichten Taneja et al. und Miles et al. in ihren Arbeiten von einer geringen Akzeptanz des Verfahrens. Diese Akzeptanz lag zwischen <20 % in Europa und Amerika sowie bis zu 60 % in Kanada [30, 31].
Da bei der Implementierung von Leitlinien in die klinische Praxis die Anwendungsraten teils stark schwanken und die Anwendung neuer Verfahren auf Widerstände stoßen können, ist es notwendig, den Prozess dauerhaft zu begleiten und weitere Schulungen anzubieten [32]. Aufgrund dieser eher ernüchternden Daten ergab sich die Fragestellung, wie es um die Akzeptanz und den Einsatz des Verfahrens in unserer Fachabteilung steht.
Die Fachabteilung für klinische Perfusion am Herz- und Diabeteszentrum Nordrhein-Westfalen (HDZ-NRW) verfügt über 23 Planstellen und 25 angestellte Perfusionisten. Um die Akzeptanz des Verfahrens in der Abteilung zu eruieren, haben wir eine anonyme Onlineumfrage mit Forms (Microsoft, USA) durchgeführt. Gleichzeitig haben wir eine Datenauswertung der Perfusionsdaten der letzten zwei Jahre seit Einführung der Dokumentation vorgenommen. Die Ergebnisse haben wir im Anschluss in Verbindung mit der Datenauswertung dazu genutzt, unser Schulungsprogramm anzupassen.
Material und Methoden
HLM-Ausstattung und Perfusionsführung
An unserem Zentrum verwenden wir die HLM S5 (LivaNova, Großbritannien), diese ist mit einer ausgelagerten ½-Zoll- Rollenpumpe, zwei ¼-Zoll-Saugerpumpen sowie einer ¼-Zoll-Doppelpumpe ausgestattet. Es kommen verschiedene Einmalsets zum Einsatz, die sich durch die eingesetzten Reservoir-/Oxygenatoreinheiten unterscheiden. Ansonsten sind sie identisch aufgebaut. Als Kardioplegieverfahren verwenden wir eine modifizierte Blutkardioplegie nach Calafiore. Zum Studienzeitpunkt wurden die Reservoir-/Oxygenatoreinheiten Inspire 8F (LivaNova, Großbritannien), FX25 (Terumo, Japan) und Alone (Eurosets, Italien) eingesetzt. Das Primingvolumen der Komplettsets unterscheidet sich nur geringfügig und beträgt ca. 1250 ml Ringer-Acetat-Lösung. Die Reduktion von überflüssigem Primingvolumen vor Beginn der Perfusion ist Bestandteil unserer Patient Blood Management-Strategie an der HLM, diese dient der Vermeidung überflüssiger Fremdblutgaben während und nach der Perfusion [18,33].
Das Vorgehen kann wie folgt beschrieben werden:
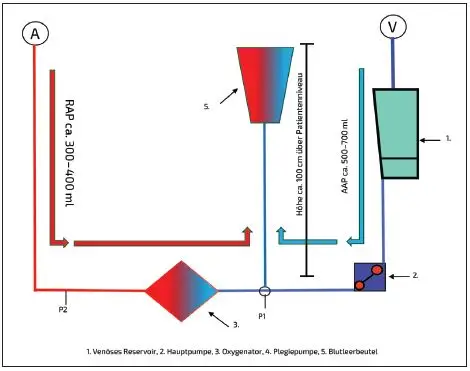
Nach systemischer Heparinisierung mit 400 IE/kg/KG und Erreichen der angestrebten Activated Clotting Time (ACT) von >480 Sekunden kann mit der Kanülierung des Patienten und der Kardiotomiesaugung begonnen werden [3]. Nach erfolgter Kanülierung und Testung der Kanülenlage wird mit dem RAP begonnen. Hierzu wird ein Blutleerbeutel mit dem Dreiwegehahn hinter der arteriellen Pumpe verbunden und der Beutel am Mast der HLM aufgehängt. Die Höhe der Aufhängung sollte etwa 1 m oberhalb des Patientenniveaus liegen. Diese Höhe ergibt sich aus der Überlegung, dass 1 cm Quecksilbersäule etwa 0,7 mmHG entsprechen. Hängt der Beutel 1 m über dem Patienten, muss der Patient mindestens ca. 70 mmHG systolischen Blutdruck aufbauen, um Blut in den Beutel zu verlieren. Theoretisch ist so ein Abfall des Patientenblutdruckes unter 70 mmHG systolisch nicht möglich. Das Verursachen eines hypovolämen Schocks durch die Volumenreduktion wird damit unwahrscheinlich. Liegt der Beutel abweichend unterhalb des Patientenniveaus, besteht die Möglichkeit eines unkontrollierten Blutverlustes mit der darauffolgenden Gefahr von Kreislaufinstabilitäten.
Durch das Öffnen des Dreiwegehahns wird nun Blut aus dem Patienten in das System und das Primingvolumen aus der arteriellen Linie und dem Oxygenator in den Blutleerbeutel geleitet [5,13,29,34–36]. In der Zwischenzeit wird vom Chirurgen die venöse Kanülierung durchgeführt. Ist der Blut- druck des Patienten weiter stabil, kann überlegt werden, ob eine antegrade Priming-Entfernung (AAP) aus der venösen Seite des Systems möglich und sinnvoll ist [35]. Über das RAP können üblicherweise 300–400 ml aus dem System entfernt werden. Toleriert der Patient das AAP ebenfalls, können hierdurch nochmals zusätzlich bis zu 700 ml aus dem System eliminiert werden (Abb. 1). Dies bietet sich vor allem bei Mitralklappen-Eingriffen in minimalinvasiver Technik mit Leistenkanülierung an. Die Reihenfolge der Kanülierung ist an unserem Zentrum in diesem Fall umgekehrt [10,37]. Die Priming-Entfernung erfolgt dann erst mittels AAP und zusätzlich RAP.
Die weitere Perfusionsführung entspricht den üblichen Standards [3]. Einziges Augenmerk sollte darauf gelegt werden, überflüssige kristalloide Volumengaben zu vermeiden. Volumen sollte nur dann verabreicht werden, wenn dies auch zwingend für die Perfusionsführung erforderlich ist. Das Be- enden der Perfusion sollte möglichst hypovoläm erfolgen. Sollte dies nicht ohne weiteres möglich sein, kann die kurzfristige Unterstützung mittels Kopftieflage oder der Gabe von Noradrenalin erwogen werden. Dies ist empfehlenswert, da nach Beendigung der Perfusion noch ca. 1250 ml Vollblut aus der EKZ zur Transfusion zur Verfügung stehen. Dieses Volumen kann dem Patienten in der Phase zwischen der venösen Dekanülierung bis zur kompletten Antagonisierung der Heparinwirkung mittels Protamin transfundiert werden. Das Restblut aus dem Oxygenator und den Schläuchen kann dem Patienten durch die Gabe von ca. 500 ml Infusionslösung in das Reservoir ebenfalls zurückgegeben werden. Der Vorteil dieses Vorgehens liegt darin, dass dem Patienten das komplette heparinisierte Blut aus der EKZ noch vor der vollständigen Protamingabe zurückgegeben werden kann. Der in dieser Phase häufig beobachtete Volumenbedarf des Patienten kann somit mit patienteneigenem Vollblut aus dem EKZ-System gedeckt werden. Das System ist danach wieder mit Infusionslösung befüllt und kann jederzeit von Neuem eingesetzt werden. In der Folge wurde das gesamte Heparin im Patienten antagonisiert. Die anschließende Kontrolle der ACT zeigt das Ergebnis nach kompletter Rückgabe des EKZ-Blutes. Hierdurch kann der gerinnungshemmende Effekt der Gabe des in einen Beutel abgefüllten EKZ-Blutes durch den Anästhesisten sowie eine potenzielle weitere Gabe von Protamin zum Ende der Operation vermieden werden.
Umfrage
Die dieser Untersuchung zugrundeliegende Umfrage wurde mit MS Forms durchgeführt. Diese bestand aus 10 Fragen (Tab. 1–3). Sie wurde den 25 Mitarbeitern der Fachabteilung per E-Mail zugesandt, und diese hatten 6 Wochen Zeit, um den Fragebogen zu beantworten. Die gewonnenen Daten wurden mit Excel und Statistical Package für Social Sciences (SPSS) der Version 29.0.2.0 aufbereitet.
Datenerhebung
Die Studie wurde als retrospektive Datenanalyse aus den Datenbanken COPRA und dem Qualitäts- und Informations- management-System (QIMS) sowie den Patientenakten im Sinne einer Matched Pair-Analyse durchgeführt. Es handelte sich um eine klinische Single-Center-Studie. Die Datenerhebung erfolgte retrospektiv aus prospektiv erhobenen Daten. Es wurden nur Patienten eingeschlossen, die einer Datenerhebung zugestimmt hatten. Die Daten wurden in pseudonymisierter Form in einer Datenbank aus QIMS, COPRA und den Patientenakten im EXCEL-Format erstellt. Die Datenanalyse wurde anonymisiert durchgeführt. Die zu untersuchenden Parameter beinhalteten prä-, intra- und postoperative Daten. Eingeschlossen wurden nur erwachsene Patienten, die im HDZ-NRW zwischen 2022 und 2023 elektiv am Herzen operiert worden sind. Es wurden 506 Patienten eingeschlossen, die im Betrachtungszeitraum einen Aorten- oder Mitralklappen-Eingriff erhalten haben. Die Gruppen ergaben sich aus dem Einsatz des Verfahrens RAP, Gruppe 1 ist die Kontroll- gruppe und Gruppe 2 ist die RAP-Gruppe.
Statistik
Die Auswertung der Daten wurde mit SPSS der Version 29.0.2.0 durchgeführt. Es wurden die Mittelwerte bestimmt und mit Standardabweichung angegeben. Die Verteilung der Daten wurde mittels Kolmogorow-Smirnow-Tests ermittelt. Die Signifikanzen wurden bei normalverteilten Daten mit dem T-Test bestimmt. Nicht normalverteilte Daten wurden mit dem Mann-Whitney-U-Test berechnet. Das Signifikanzniveau wurde mit 0,05 festgelegt. Nominale Daten wurden mit Anzahl und Prozent angegeben. Die Signifikanzen wurden bei diesen mit dem Chi-Quadrat-Test berechnet.
Ergebnisse
Umfrage
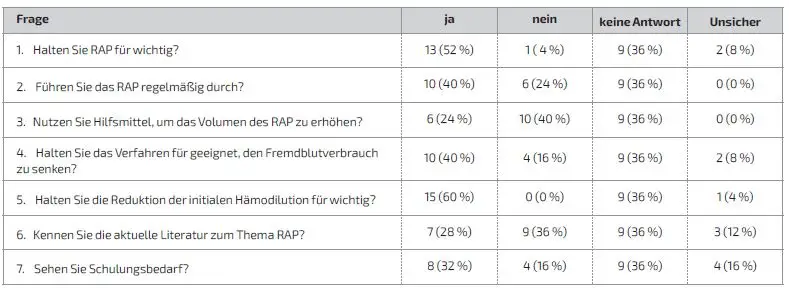
In unserer Fachabteilung waren zum Umfragezeitpunkt 25 Kollegen angestellt. Diese wurden zur Umfrage eingeladen. Es haben 16 (64 %) Personen in der vorgegebenen Zeit geantwortet. 9 (36 %) haben nicht teilgenommen. Von den teilnehmenden Kollegen hielten 13 (52 %) das Verfahren RAP dabei für wichtig. Dies deckt sich mit der Annahme, dass die Reduktion der initialen Hämodilution für 15 (60 %) der Befragten ein wichtiger Punkt ist.
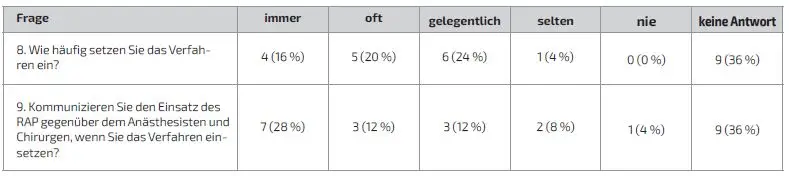
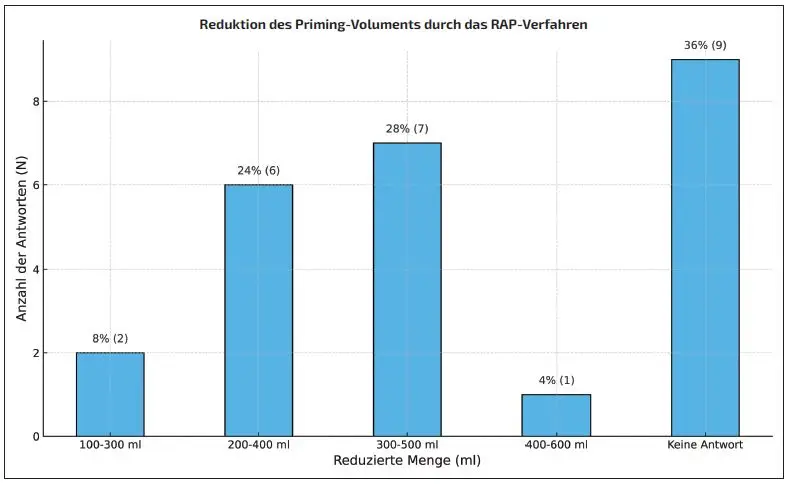
Weitere 10 (40 %) Kollegen haben angegeben, das Verfahren regelmäßig anzuwenden (Tab. 1). Die Menge der Reduktion des Primingvolumens wurde von 13 (52 %) Kollegen mit 200–500 ml angegeben (Abb. 2). Vier (16 %) Kollegen haben angegeben, das Verfahren immer zu verwenden. Weitere 5 (20 %) Kollegen gaben an, es oft einzusetzen (Tab. 2). Das Nutzen von Hilfsmitteln, wie der Kopftieflagerung des Patienten oder der Einsatz von Noradrenalin zur Erhöhung des RAP-Volumens wurde von 6 (24 %) Kollegen angegeben. 10 (40 %) Kollegen setzten keine Hilfsmittel ein (Tab. 1). Die Durchführung des Verfahrens wurde von 13 (52 %) der Befragten an die Anästhesie und an den Chirurgen kommuniziert. 3 (12 %) der Befragten gaben an, dies selten oder nie zu kommunizieren (Tab. 2). Die Möglichkeit, den Fremdblutbedarf durch den Einsatz des Verfahrens zu senken sahen 10 (40 %) Kollegen, 6 (24 %) Kollegen sahen diese Möglichkeit nicht oder waren sich unsicher, ob dies so ist. Die Frage nach der Kenntnis der aktuellen Literatur zum Thema wurde von 7 (28 %) Kollegen mit ja beantwortet. 12 (48 %) gaben an, diese entweder nicht zu kennen oder waren sich unsicher. Abschließend wurde gefragt, ob es einen Schulungsbedarf zu diesem Thema in der Abteilung gibt. Diesen sahen 8 (32 %) der Befragten (Tab. 1).
Datenauswertung
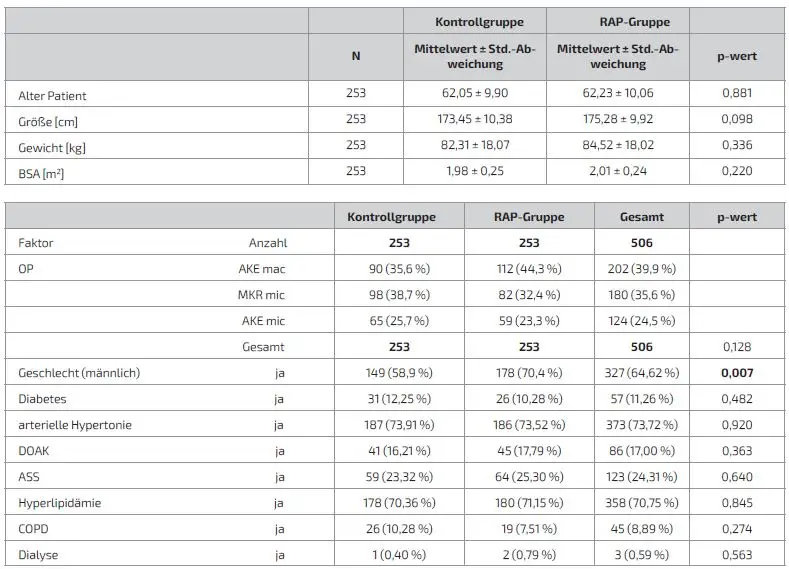
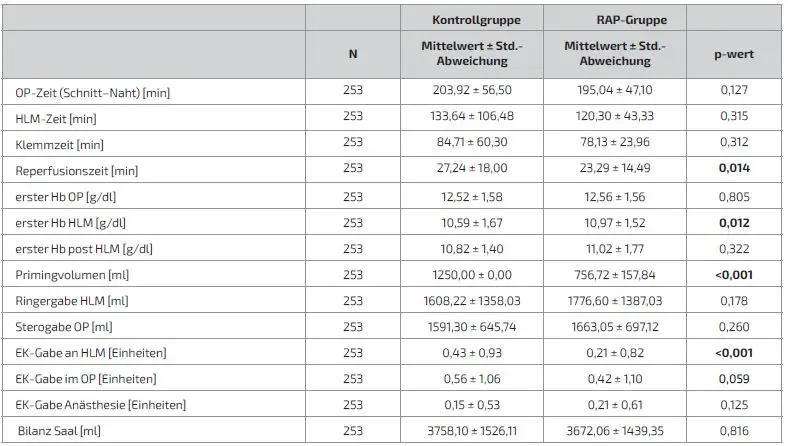
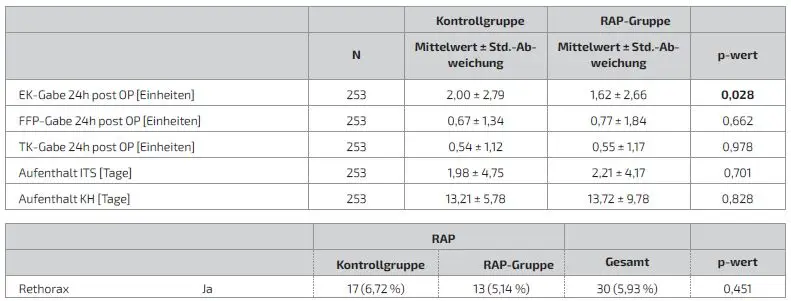
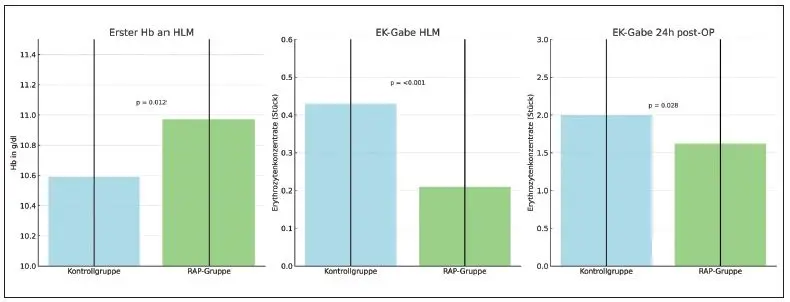
Insgesamt konnten 506 Patienten in die Auswertung eingeschlossen werden. 253 Patienten wurden der Kontrollgruppe, 253 der RAP-Gruppe zugeordnet. Die gesamten demografischen Daten sind in Tabelle 3 dargestellt. Diese wiesen keine signifikanten Unterschiede auf, bis auf das Geschlecht, 149 (58,9 %) männliche Patienten in der Kontrollgruppe zu 178 (70,4 %) männliche Patienten in der RAP- Gruppe, p = 0,007. Bei den intraoperativen Daten, dargestellt in Tabelle 4, zeigten sich signifikante Unterschiede (in der Tabelle fettgedruckt) bei der Reperfusionszeit mit 27,24 ± 18,0 Minuten in der Kontrollgruppe zu 23,29 ± 14,49 Minuten in der RAP-Gruppe, p = 0,014. Der erste Hb nach dem Beginn des Bypasses war mit 10,97 ± 1,52 g/dl höher als in der Kontrollgruppe mit 10,59 ± 1,67 g/dl, p = 0,012. Weitere Unterschiede ergaben sich beim Primingvolumen aufgrund des Gruppenunterschiedes in der Kontrollgruppe mit 1250 ml ± 0,0 zu der RAP-Gruppe mit 756,27 ± 157,84 ml, p = <0,001. Ebenfalls unterschiedlich waren die EK-Gabe an der HLM mit 0,43 ± 0,93 der Kontrollgruppe zu 0,21 ± 0,82 Erythrozytenkonzentraten in der RAP-Gruppe, p = <0,001. Die restlichen Werte hatten keine signifikanten Unterschiede. Bei den postoperativen Daten, dargestellt in Tabelle 5, zeigten sich signifikante Unterschiede bei der EK-Gabe in den ersten 24 Stunden postoperativ mit 2,0 ± 2,79 Erythrozytenkonzentraten in der Kontrollgruppe zu 1,62 ± 2,66 Erythrozytenkonzentraten in der RAP-Gruppe, p = 0,028. Die restlichen unter- suchten Werte wiesen keine signifikanten Unterschiede auf.
Diskussion
Die Umfrage zur Akzeptanz des Verfahrens hatte eine Laufzeit von 6 Wochen. Die Rücklaufquote war mit 64 % geringer als erwartet. Damit können wir auf ein Drittel der Belegschaft keine Rückschlüsse ziehen. Von den restlichen Kollegen halten 52 % das Verfahren des RAP für wichtig oder sinnvoll. 60 % sehen in der Reduktion der initialen Hämodilution einen wichtigen Punkt. 40 % der Kollegen führen das RAP regelmäßig durch. Leider geben 48 % der Teilnehmer an, dass die aktuelle Literatur nicht bekannt ist. Sehr positiv kann allerdings bewertet werden, dass 48 % der Befragten einen Schulungsbedarf sehen oder sich in dieser Frage unsicher sind. Dies könnte ebenfalls mit dem Anteil der Kollegen, die das Verfahren nicht anwenden bzw. nicht an der Umfrage teilgenommen haben, korrelieren und einen wichtigen Ansatzpunkt für weitere interne Schulungen darstellen.
Bezüglich der klinischen Wirksamkeit des Verfahrens haben wir eine Datenbankabfrage durchgeführt. Ziel war es, die Effektivität des Verfahrens an unserem Hause zu untersuchen und eine interne Datenbasis für weitere Schulungen zu schaffen. Wir konnten in der RAP-Gruppe eine mittlere Reduktion des Primings auf 756 ± 157 ml nachweisen. Dies entspricht etwa 500 ml Reduktion und ist unserer Meinung nach ein sehr guter Wert. Wie bereits von Moscarelli et al. beschrieben [37], lässt sich das Verfahren bei minimalinvasiven Mitralklappen-Eingriffen besonders effektiv mit dem AAP kombinieren. Hierdurch entstehen deutlich höhere Priming-Reduktionen und geringere Hämoglobinabfälle bei der Initiierung der HLM. In der Folge konnten wir mit unseren Ergebnissen den Effekt der Verringerung der initialen Hämodilution, die Reduktion des Fremdblutverbrauchs an der HLM und im 24 h-Verlauf bestätigen (Abb. 3) [1,2]. Auf die Parameter des Aufenthaltes auf der Intensivstation und im Krankenhaus hatte das RAP in unserer Untersuchung, wie bereits von Hensley et al. beschrieben, ebenfalls keinen Effekt [2]. Diese Ergebnisse bestärken uns allerdings in der Überzeugung, dass dieses Verfahren ein wertvoller Baustein des PBM ist. Die Herausforderung besteht allerdings darin, dass eine offensichtliche Reduktion von Bluttransfusionen nicht zwingend ein besseres Outcome zur Folge haben muss. Sinnvoll wäre es daher, ein Gesamtkonzept mit der Anästhesieabteilung und den postoperativ verantwortlichen Intensivmedizinern zu etablieren. Das Ziel sollte es sein, den Fremdblutverbrauch auf ein medizinisch notwendiges Minimum zu reduzieren. Grundlegende Forschungen und Betrachtungen der medizinischen Notwendigkeit sowie Verträglichkeit niedriger Hämoglobinkonzentrationen liegen hierzu von der Arbeitsgruppe um Zacharowski et al. vor [18,33] und werden weiter untersucht.
Wird ein konsequentes PBM durchgeführt, sollte dies theoretisch an sich schon zu einer Reduktion des messbaren Fremdblutverbrauches an der HLM führen. In der Folge wären die harten Fakten, die für das RAP sprechen, reduziert. Dies sollte aber nicht dazu führen, auf eine konsequente Reduktion der initialen Hämodilution zu verzichten. Bereits 2019 wurde das Verfahren des RAP von Wahaba et al. in der CPB-Guideline [3] und der PBM-Guideline 2024 [4] (Class 1, Level of Evidence A) empfohlen. Dieser Empfehlung folgend, sehen wir es daher als sinnvoll an, die Durchführung durch alle Kollegen der Abteilung zu fördern und zu fordern. Zusammenfassend ist allerdings festzustellen, dass die Implementierung bislang nur von 50 % der Mitarbeiter betrieben wurde. Hieraus ergibt sich für uns die Notwendigkeit, die Implementierung mit weiteren Schulungen und Praxisanleitungen zu begleiten und eventuell bestehende Hürden oder Ängste im Zusammenhang mit der Methode abzubauen.
Schlussfolgerung
Das Verfahren des RAP ist ein etabliertes Standardverfahren, das bislang noch nicht vollständig in der Klinik angekommen ist. Es ist zwar relativ einfach anzuwenden, es bestehen jedoch offensichtlich gewisse Hürden, dieses auch konsequent anzuwenden. Es scheint daher geboten, das Verfahren im Rahmen bestehender oder neu zu etablierender PBM-Strategien und daraus entstehender Verfahrensanweisungen in der Klinik weiter zu etablieren und die Anwendung zu fördern.
Limitationen
Die Rücklaufquote der Umfrage lag lediglich bei 64 %. Mit nur 16 Antworten ist die Aussagekraft der Umfrage somit stark eingeschränkt. Die Möglichkeit einer Verzerrung durch Selbstselektion ist hoch und die Generalisierbarkeit der Ergebnisse ist fraglich. Eine höhere Teilnahmequote wäre wünschenswert gewesen, um belastbarere Aussagen treffen zu können. Der retrospektive Charakter dieser Single-Center-Studie ist in ihrer Generalisierbarkeit eingeschränkt, da die Ergebnisse nur für unser Zentrum gelten und nur bedingt auf andere Einrichtungen übertragbar sind. Zudem besteht eine potenzielle Verzerrung der Patientenselektion, da die Patientenauswahl rückblickend erfolgt und bestimmte Gruppen möglicherweise unterrepräsentiert sind. Unvollständige oder fehlerhafte Daten sowie fehlende Kontrolle über Störfaktoren können die Validität der Ergebnisse beeinträchtigen. Da nur dokumentierte Fälle analysiert werden, kann es zu einer Beeinflussung der Ergebnisse kommen und aufgrund des retrospektiven Designs sind kausale Zusammenhänge nicht sicher nachweisbar.
Ethische Aspekte
Die Studie wurde in Übereinstimmung mit der Deklaration von Helsinki durchgeführt und von der Ethikkommission der Medizinischen Fakultät der Ruhr-Universität Bochum mit Sitz in Ostwestfalen, Protokollcode 2025-1330 am 30.01.2025, genehmigt.
Interessenkonflikte
Die Autoren geben an, keine Interessenkonflikte zu haben.







