EINLEITUNG
Die Neigung zu Ödemen ist ein bekanntes Problem bei Patient:innen mit einem ExtraCorporeal Life Support (ECLS)-System. Dies tritt sowohl bei Erwachsenen als auch bei pädiatrischen Patient:innen auf und kann durch eine Niereninsuffizienz verstärkt werden bzw. bildet die Grundlage für diese [1–5]. Eine länger andauernde eingeschränkte Diurese erfordert insbesondere bei Säuglingen therapeutische Maßnahmen, um eine weitere Überwässerung und Intoxikation zu verhindern. Klassische Nierenersatzverfahren sind die Hämofiltration (HF) und die Hämodiafiltration (HDF) über einen Sheldon-Katheter an einem separaten Hämofiltrationsgerät mit einem großen extrakorporal zirkulierenden Volumen. Alternativ wird in dieser Patientenkohorte die Peritonealdialyse eingesetzt mit dem möglichen Nachteil, dass die zugeführte Dialyseflüssigkeit im Bauchraum auf vorgeschädigte Organe nachteilig wirkt.
FALLBERICHT
Wir berichten von einem 8 Tage alten Säugling mit einer Transposition der großen Arterien (TGA-Stellung) und einem Körpergewicht von 2,7 kg nach arterieller Switch-Operation. Die Korrekturoperation mit EKZ wurde in einer Bypasszeit von 308 min mit 170 min Ischämiezeit durchgeführt. Nach komplikationslosem Abgang von der EKZ und Verlegung auf die Intensivstation verschlechterte sich der Zustand des Patienten in der ersten postoperativen Nacht. Es kam zu einem ausgeprägten SIRS mit Low-Cardiac-Output-Syndrom, so dass eine ECLS-Implantation erforderlich wurde.
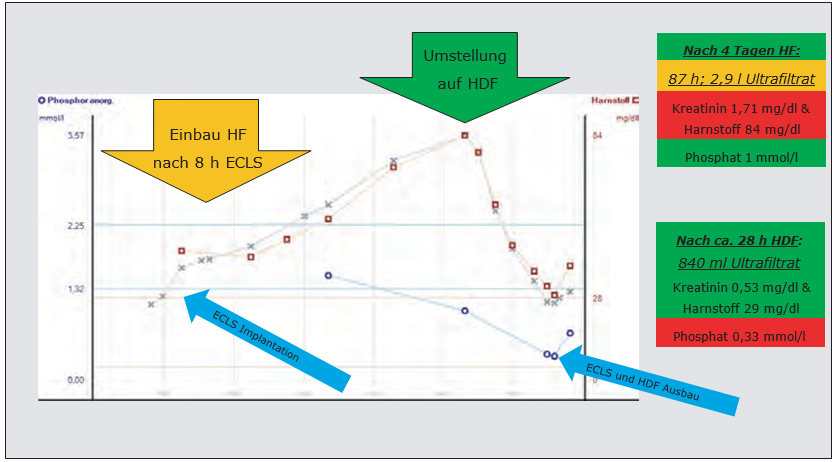
Trotz adäquatem HZV unter ECLS-Therapie bestand auch 8 Stunden nach Implantation immer noch eine Anurie mit Ödemen, was die Indikation für eine minimierte Hämofiltration am ECLS darstellte. Das in diesem Fall neuartige Hämofiltrations-System bestand bei diesem ersten Fall aus mehreren Komponenten: ein Infusomat Space P (B. Braun, Melsungen, Deutschland), 2 * Heidelberger Verlängerungen (Fresenius Kabi, Bad Homburg, Deutschland) und einem Hämofilter HPH Junior (Terumo Corp, Tokyo, Japan). Der Hämofilter hatte eine Membranoberfläche von 0,09 m² und 8 ml Priming. Das Primingvolumen für das gesamte Hämofiltrationssystem umfasste 28 ml. Das Hämofiltrationssystem wurde blutseitig als druckabhängiger Bypass in das ECLS integriert. Wie in Abbildung 1 grün dargestellt, wird das Blut aus dem Oxygenator kommend zum Hämofilter geleitet und passiv in den venösen Schenkel vor die ECLS-Pumpe rückgeführt. Links im Bild ist die blutseitige Überwachung des Bypassflusses des Hämofiltrationsystems (Abb. 1) zu sehen. Die Regulierung der Menge des Ultrafiltrats erfolgte über den Infusomaten (30 ml/h). Über die Dauer von 87 Stunden erfolgte eine kontrollierte, den hämodynamischen Verhältnissen angepasste, Hämofiltration. Insgesamt konnten bis zu diesem Zeitpunkt 2,9 l Ultrafiltrat gewonnen werden.

Trotz HF kam es zu steigenden Retentionswerten mit einem maximalen Kreatinin von 1,71 mg/dl und einem Harnstoff von 84 mg/dl. Daraufhin erweiterten wir die reine HF um einen zweiten Infusomaten mit 200 ml/h Dialysatfluss im Gegenstromprinzip zu einer HDF. Der Abnahmefluss am Dialysatinfusomat musste daraufhin um diese 200 ml/h auf 230 ml/h angepasst werden, um eine effektive Abnahme von 30 ml/h zu erreichen (Abb. 2). Während der folgenden 28 Stunden dauernden HDF konnten die Retentionswerte effektiv gesenkt werden. Das Kreatinin fiel auf 0,53 mg/dl und der Harnstoff auf 29 mg/dl. Bei dann verbesserter kardialer Funktion und wiedereinsetzender Diurese konnte das ECLS-System erfolgreich explantiert werden.
Wir konnten bei der Behandlung mittels HDF das Auftreten einer behandlungswürdigen Hypophosphatämie detektieren. Nach der HF war der Phosphatwert bei 1 mmol/l und wurde durch die HDF auf 0,33 mmol/l gesenkt (Abb. 2).
DISKUSSION
Die Indikation zu einer perioperativen ECMO-Therapie bei herzchirurgischen Eingriffen wird mit 2,8 % angegeben [6]. In einer multizentrischen Studie mit 357 pädiatrischen ECMO-Patient:innen zeigten 72 % ein behandlungswürdiges akutes Nierenversagen. Darüber hinaus bezeichnen Gorga et al. das Überwässern von pädiatrischen Patient:innen am ECMO-System als einen unabhängigen Faktor für Krankenhausüberleben [1]. In einer aktuellen Studie aus 2022, an der 60 pädiatrische Einrichtungen teilnahmen, zeigte sich, dass in 45 % der Einrichtungen die konventionelle Dialyseeinheit, in 8 % der Fälle eine in-line-Hämofiltration und in den restlichen Kliniken eine Kombination aus verschiedenen Dialyseverfahren während der ECMO-Therapie Anwendung findet [2]. Im vorliegenden Fall hatten wir neben der Anurie eine starke Hyperhydration am laufenden ECLS-System, was die Indikation für ein Nierenersatzverfahren bedeutete.
Das Körpergewicht war mit 2,7 kg sehr niedrig und die Zugänge für konventionelle Therapieverfahren äußerst limitiert. Dadurch stellte das Behandlungsteam, das über Erfahrung mit dem Anschluss von Dialysegeräten an größere ECLS-Systeme [3] verfügt, nach innerklinischer Beratung erstmals die Indikation, ein hausinternes, minimiertes pädiatrisches Hämofiltrationssystem zum Volumenentzug am laufenden ECLS-System zu implementieren.
Nach der anfänglichen Euphorie, dass wir mit dem einfachen HF-System eine optimale Entwässerung des kleinen Neugeborenen erreichten, mussten wir feststellen, dass wir mit dem Verfahren keine ausreichende Clearence erreichen konnten. Daraufhin wurde nach Rücksprache mit der nephrologischen Abteilung eine Erweiterung des Systems durchgeführt, was die gewünschte Reduktion der Retentionswerte hervorbrachte (Abb. 3).

Die Überwachung und notfalls Behandlung von niedrigen Phospatwerten (Normwert: 0,9–2,9 mmol/l) ist essenziell, da Phosphat ein wichtiger Energielieferant für ATP ist. Ein schwerer Phosphatmangel kann u. a. neben Verwirrtheit zu epileptischen Anfällen, Koma, einem gestörten Atemantrieb, verringerter Darmtätigkeit und zu einer perioperativen Schwächung des Herzmuskels führen [7].
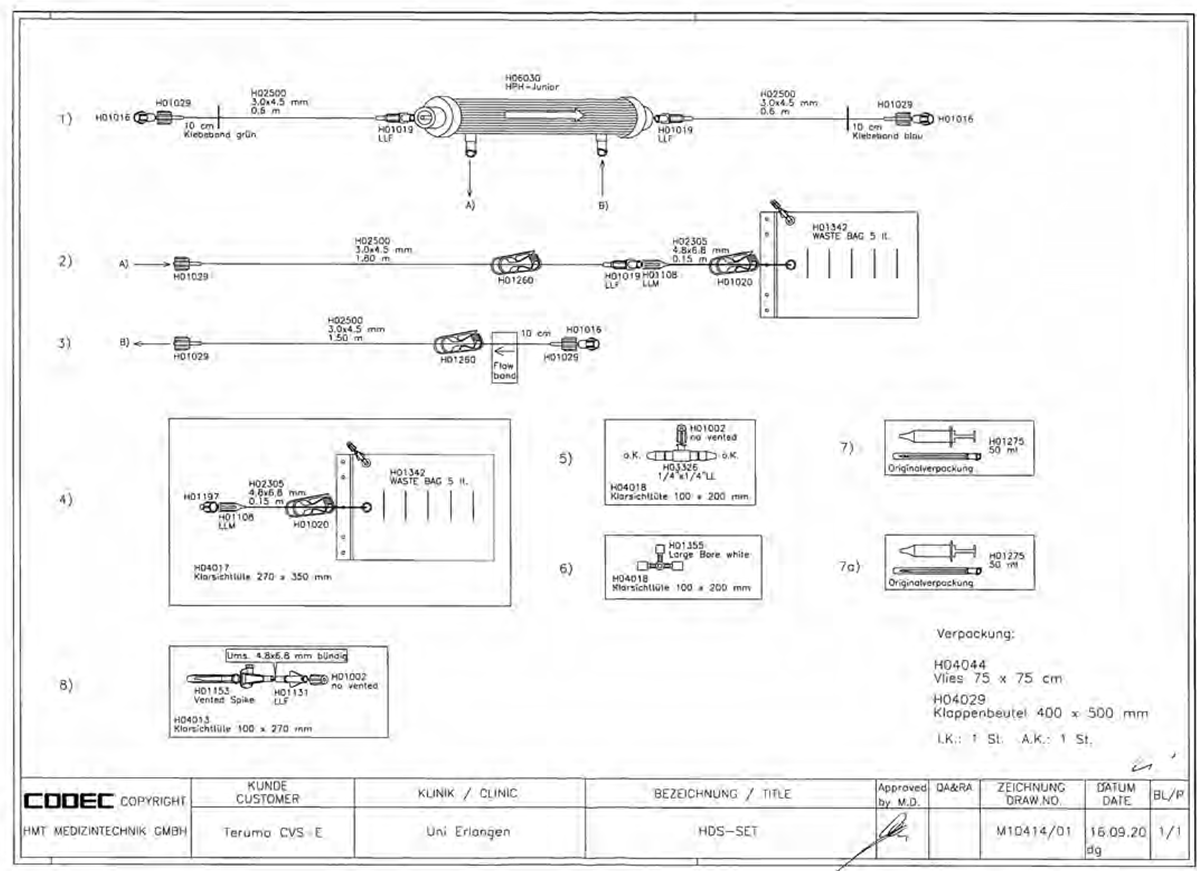
Nach diesem ersten Fall wurde im Perfusionsteam ein kundenspezifisches Hämodiafiltrationssystem entwickelt. Das mit 18 ml blutseitige Priming inklusive dem Hämofilter kann zu Recht als minimiertes pädiatrische Hämodiafiltration bezeichnet werden (Abb. 4). Die Einsatzzeit bis zum Wechsel des HDF-Systems, bei laufendem ECLS-System oder ECMO, wurde nach den erlaubten Einsatzzeiten von käuflich zu erwerbenden Standard-HDF-Schlauchsets zur Blutreinigung übernommen. Die Einsatzzeit des HDF-Systems ist auf maximal 72 Stunden begrenzt [8]. Diese maximale Einsatzzeit von 72 Stunden wurde daraufhin in der internen SOP für die Behandlung von HDF an der ECMO festgelegt.
SCHLUSSFOLGERUNG
Ein effektiver Einsatz eines minimierten Hämofiltrationsverfahrens zum Volumenentzug am ECLS-System ist technisch unproblematisch durchführbar. Die Erweiterung der Hämofiltration zu einer Hämodiafiltration ermöglicht eine effektive Elimination harnpflichtiger Substanzen. Neben der Überwachung der Retentionsparameter ist bei der Hämodiafiltration die Kontrolle des Phosphathaushalts erforderlich. Ein adäquater Volumenentzug bei überwässerten Säuglingen mit Anurie bei laufendem ECLS ist so methodisch möglich – bei stark reduziertem Primingvolumen im Vergleich zu einem konventionellen Dialysegerät. Auf einen zusätzlichen Sheldon-Katheter zur Dialyse kann hierbei verzichtet werden. Somit stellt der Anschluss einer minimierten Hämodiafiltration eine unkomplizierte und schonende Alternative zu konventionellen Nierenersatzverfahren dar.
INTERESSENKONFLIKT
Die Autoren haben keine relevanten Interessenkonflikte im Rahmen der vorliegenden Publikation.







