Einleitung
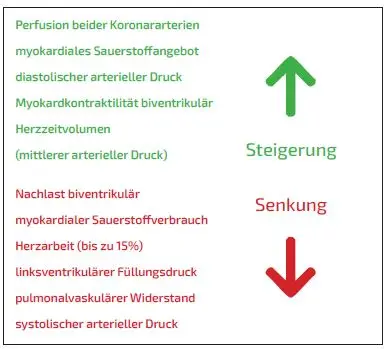
Die intraaortale Gegenpulsation, realisiert durch eine intraaortale Ballonpumpe (IABP), hat sich seit ihrer klinischen Einführung 1963 durch Kantrowitz zu dem technisch einfachsten und weltweit am häufigsten eingesetzten mechanischen Kreislaufunterstützungssystem entwickelt [1]. Nach Einbringen eines Ballonkatheters in die Aorta descendens distal des Abganges der linksseitigen Arteria subclavia wird dieser synchronisiert zur Herzaktion – getriggert durch Elektrokardiogramm (EKG) oder arterielle Druckkurve – über eine externe Pumpe mit ca. 30–50 cm3 Helium gefüllt. Dabei wird der Ballon unmittelbar nach Schluss der Aortenklappe zu Beginn der Diastole (Dikrotsche Inzisur in der arteriellen Druckkurve) insuffliert. Dabei wird eine Pulswelle antegrad sowie retrograd (also herzwärts gerichtet in Richtung Aortenklappe) ausgelöst. Dadurch wird bei kompetenter Aortenklappe eine Verbesserung der Koronarperfusion erreicht. Diese wird auch als diastolische Gegenpulsation oder Augmentation bezeichnet und bewirkt ein gesteigertes links- wie rechtsventrikuläres Energieangebot für das Myokard. Das unmittelbar präsystolische Leersaugen des Ballons bewirkt eine Senkung der linksventrikulären Nachlast mit konsekutiver Reduktion der linksventrikulären Wandspannung und des linksventrikulären enddiastolischen Druckes. Hieraus resultiert eine Reduktion des myokardialen Sauerstoffverbrauches (Abb. 1).
Im Jahr 2015 wurde erstmals eine S3-Leitlinie unter Federführung der Deutschen Gesellschaft für Herz-, Thorax- und Gefäßchirurgie (DGTHG) „Einsatz der intraaortalen Ballongegenpulsation in der Herzchirurgie“ erstellt und veröffentlicht. Diese Leitlinie wurde nun einer Aktualisierung und Überarbeitung unterzogen. In den letzten Jahren ist die Einordnung und Nutzung der IABP in der Herzchirurgie im Wesentlichen durch zwei Aspekte geprägt:
- dem fehlenden Nachweis einer Überlegenheit der IABP gegenüber bestmöglicher medikamentöser Behandlung im Kontext der vornehmlich interventionellen Revaskularisation bei kardiogenem Schock [2]
- der zunehmenden Verfügbarkeit aktiver mechanischer Kreislaufunterstützungsverfahren wie extrakorporale Membranoxygenierung/extracorporeal life support (ECMO/ECLS) oder Mikroaxialpumpen (z. B. Impella, Abiomed)
Vor diesem Hintergrund wurde die Leitlinie zwischen 2020 und 2024 unter Mitwirkung aller mit der Versorgung von Herzpatienten betrauten Fachgesellschaften überarbeitet. Grundlegende Neuerungen im Rahmen der Überarbeitung sind: Die Leitlinie wurde neu in die vier Themenkomplexe „Therapeutische IABP“, „Prophylaktische IABP“, „Management der IABP“ und „IABP im Kontext anderer mechanischer Kreislaufunterstützungsverfahren“ gegliedert. Zu allen Themenkomplexen wurden Schlüsselfragen formuliert und die Empfehlungen als Antworten auf diese Schlüsselfragen konzipiert. Die aktuelle Evidenz wurde erfasst, bewertet und in die aktualisierten Empfehlungen eingebunden. Die aktualisierte Version der Leitlinie enthält zudem erstmals Empfehlungen zu pflegerischen Aspekten der IABP-Therapie. Im Folgenden sollen die Ergebnisse der Statuserhebung zur aktuellen IABP-Nutzung sowie die Kernaussagen und Empfehlungen der neuen Leitlinienversion zusammengefasst werden. Detaillierte Informationen zur Methodik der Leitlinienerstellung finden sich auf den Seiten der Arbeitsgemeinschaft der wissenschaftlichen medizinischen Fachgesellschaften e. V. [3].
Gegenwärtige Anwendung der IABP in der Herzchirurgie
Eine 2009 vor Erstellung der Erstversion der S3-Leitlinie durchgeführte Umfrage in den herzchirurgischen Kliniken in Deutschland zeigte eine heterogene Anwendungspraxis der IABP [4]. Vor Beginn der Aktualisierung der Leitlinie wurde erneut eine Umfrage in den 78 herzchirurgischen Kliniken in Deutschland zur Nutzung der IABP durchgeführt. Die Umfrage bestand aus einem Online-Fragebogen mit 18 Items. 53 der 78 angeschriebenen Kliniken (63 %) nahmen an der Umfrage teil. Hierbei gaben 53 % der Zentren an, dass die Anwendungshäufigkeit der IABP im Vergleich zum Vorjahr abgenommen habe, 35 % berichteten über unveränderte Anwendungszahlen, bei 12 % habe die Häufigkeit zugenommen. Bezüglich der Standardisierung der IABP-Anwendung berichteten 14 % der Zentren, dass ein kriteriengestütztes Protokoll bestehe, während 61 % der Zentren angaben, die Anwendung der IABP werde nach Maßgabe des behandelnden Chirurgen eingesetzt. 89 % der Zentren gaben den Eindruck an, dass die Anwendung der IABP seit 01/2015 zu Gunsten anderer Unterstützungsverfahren rückläufig sei. Als derzeit wichtige Alternativen zur IABP wurden (bei Mehrfachnennungsmöglichkeit) ECLS (76 %), Impella 5.0/5.5 (52 %), Impella CP (39 %), Impella 2.5 (41 %) und TandemHeart (3 %) genannt. Die grundsätzliche Akzeptanz der IABP als therapeutisches Verfahren durch kardiologische Partner im Herz-Team wurde durch die chirurgischen Zentren so empfunden, dass die IABP größtenteils als überflüssig an- gesehen werde (53 %) oder nicht als Unterstützungsoption angesehen werde (20 %). In 24 % der Zentren würden jedoch teilweise Indikationen für die IABP anerkannt. Die Frage, ob die Erstversion dieser Leitlinie die Praxis der IABP-Anwendung in den Zentren verändert habe, bejahten 37 % der Zentren, 61 % verneinten die Frage und 2 % gaben an, ihnen sei die Leitlinie nicht bekannt. Die Ergebnisse dieser Umfrage wurden von der Leitliniengruppe als Auftrag interpretiert, in der aktualisierten Leitlinienversion einen verstärkten Fokus auf die Anwendung der IABP im Kontext der anderen verfügbaren mechanischen Kreislaufunterstützungsverfahren (mechanical circulatory support, MCS) zu legen.
Die IABP als therapeutisches Unterstützungsverfahren
Unter „therapeutischer IABP“ wird eine IABP-Anwendung zur akuten Behandlung einer hämodynamischen Störung definiert. Im Unterschied dazu wird die „prophylaktische IABP“ als IABP-Behandlung zur Vermeidung antizipierter hämodynamischer Störungen definiert.
Schlüsselfrage 1: Soll die IABP bei infarktbedingtem kardiogenem Schock eingesetzt werden?
Der kardiogene Schock (cardiogenic shock, CS) ist ein komplexes Syndrom, das zu Beginn einer Kaskade aus eingeschränkter kardialer Pumpfunktion, Hypotension und verminderter Gewebeperfusion steht [5]. Sekundär kommt es im Rahmen eines Ischämie-Reperfusionsschadens zu einer systemischen Inflammationsreaktion mit Freisetzung proinflammatorischer Zytokine, Expression der induzierbaren NO-Synthase und einer inadäquaten Vasodilatation sowie zu einem Multiorganversagen [5]. Der infarktbedingte CS war über Dekaden hinweg die Hauptindikation zur Implantation der IABP im Bereich der Kardiologie. So empfahlen sowohl die AHA/ACC als auch die ESC in ihren früheren Leitlinien zur Therapie des ST-Hebungsinfarkts (STEMI) im Falle des kardiogenen Schocks den Einsatz der IABP mit einer Klasse I-Indikation [6,7]. Im Bereich der Kardiochirurgie existieren keine randomisiert-kontrollierten Studien (randomized-controlled trials, RCT) zum Einsatz der IABP beim infarktbedingten kardiogenen Schock. Die bisher größte randomisierte Studie zum Einsatz der IABP im infarktbedingten kardiogenen Schock wurde 2012 publiziert: Im Rahmen des IABP-SHOCK-II-Trial wurden im Zeitraum von Juni 2009 bis März 2012 600 Patienten mit kardiogenem Schock als Folge eines Myokardinfarktes, die eine frühe Revaskularisation erhielten, an 37 deutschen Zentren entweder nur intensivmedizinisch behandelt oder sie erhielten zusätzlich eine IABP. Der primäre Studienendpunkt, die 30-Tage-Sterblichkeit, war in beiden Studienarmen mit 39,7 % im IABP-Arm und 41,3 % im Kontrollarm vergleichbar. Ebenso zeigte sich in keinem anderen untersuchten Endpunkt (Kreislaufparameter, Nierenfunktion, intensivmedizinische Behandlungstage, Beatmungstage, etc.) ein Vorteil für die IABP, allerdings auch keine Häufung von Komplikationen, wie etwa Blutungen. Auch die Analyse der Per-Protokoll-Population und eine Multivarianzanalyse sowie eine umfangreiche Subgruppenanalyse ergaben keine relevanten Sterblichkeitsunterschiede zwischen beiden Gruppen. Die Ergebnisse konnten auch im Langzeit-Follow-up nach 12 Monaten und 6 Jahren bestätigt werden [8,9].
Die Übertragbarkeit auf den herzchirurgischen Kontext aller randomisierten Daten zur IABP im infarktbedingten kardiogenen Schock einschließlich des IABP-SHOCK-II-Trials ist durch den sehr geringen Anteil der Patienten, die primär einer chirurgischen Koronarrevaskularisation zugeführt wurden, limitiert. So lag der Anteil der chirurgisch versorgten Patienten im IABP- SHOCK-II-Trial unter 4 %. Eine rein kardiochirurgische, randomisierte Untersuchung zu dieser Thematik existiert nicht und die Ergebnisse einer Studie mit nahezu ausschließlich interventionell revaskularisierten Patienten können nicht uneingeschränkt auf kardiochirurgische Patienten übertragen werden. Aus dem herzchirurgischen Bereich existieren mehrere Registerstudien, die aber aufgrund ihres Alters und des Studiendesigns inherenten Limitationen nur sehr eingeschränkte Aussagekraft aufweisen [10–12].
Schlüsselfrage 2: Soll die IABP bei dekompensierten Klappenvitien (Mitralklappeninsuffizienz, Aortenklappenstenose) eingesetzt werden?
Grundsätzlich erscheint die IABP bei dekompensierter Aortenklappenstenose oder Mitralklappeninsuffizienz sinnvoll: Im Rahmen einer akuten kardialen Dekompensation bei Aortenklappenstenose oder Mitralklappeninsuffizienz stehen eine Nachlastreduktion sowie eine Steigerung der Kontraktilität im Vordergrund. Die IABP stellt somit mit ihren beiden Haupteffekten – der Nachlastsenkung sowie Steigerung der Koronarperfusion – vom physiologischen Verständnis her eine sinnvolle Therapieoption bei Patienten mit dekompensierter Aortenklappenstenose oder Mitralklappeninsuffizienz dar. Die Evidenz beschränkt sich auf eine retrospektive Studie mit 25 eingeschlossenen Patienten [13].
Schlüsselfrage 3: Soll die IABP bei mechanischen Komplikationen des akuten Myokardinfarkts eingesetzt werden?
Bei mechanischen Komplikationen des akuten Myokardinfarkts (Infarkt-Ventrikelseptumdefekt (VSD), Papillarmuskelabriss der Mitralklappe mit akuter Mitralklappeninsuffizienz) könnte die IABP durch Nachlastsenkung und Verbesserung der Koronarperfusion einen Vorteil bringen. Die IABP zeigte in mehreren Studien eine hämodynamische Stabilisierung bei Patienten mit infarktbedingtem VSD oder Mitralklappeninsuffizienz, jedoch ohne nachgewiesenen Überlebensvorteil. Retrospektive Untersuchungen berichten von positiven Effekten der IABP, wobei die Ergebnisse stark vom Operationszeitpunkt abhängen und frühzeitige Eingriffe mit höherer Mortalität verbunden sind. Eine große Analyse mit 2876 Patienten zeigte, dass die IABP häufiger bei kritisch kranken Patienten eingesetzt wurde, was die Interpretation der Ergebnisse erschwert. Insgesamt fehlen prospektiv-randomisierte Studien zur IABP bei mechanischen Infarktkomplikationen, wodurch endgültige Schlussfolgerungen limitiert sind [14–16].
Schlüsselfrage 4: Soll die IABP bei Rechtsherzinsuffizienz eingesetzt werden?
Den hämodynamischen Effekten der IABP folgend, erscheint der Einsatz der IABP im Rahmen der akuten Rechtsherzinsuffizienz rational: Aufgrund der gesteigerten Koronarperfusion kann es zu einer rechtsventrikulären Inotropiesteigerung kommen, eine rechtsventrikuläre Nachlastsenkung entspricht einer Senkung des pulmonalvaskulären Widerstandes. Es gibt nur wenige klinische Daten zur Nutzung der intraaortalen Ballonpumpe (IABP) bei akutem Rechtsherzversagen, jedoch zeigen Fallberichte und retrospektive Studien eine hämodynamische Stabilisierung durch eine Senkung der Füllungsdrücke und eine Verbesserung des Herzzeitvolumens [17,18]. Tierexperimentelle Studien bestätigen den potenziellen Nutzen der IABP, insbesondere in Kombination mit Vasopressoren, da eine alleinige IABP-Therapie nicht immer ausreicht, um die rechts- ventrikuläre Funktion signifikant zu verbessern [19].
Schlüsselfrage 5: Soll die IABP bei akuter Dekompensation einer chronischen Herzinsuffizienz eingesetzt werden?
Die IABP könnte bei akuter Dekompensation einer chronischen Herzinsuffizienz als Überbrückungsmaßnahme hin zu einer Stabilisierung bzw. Erholung eingesetzt werden. Mehrere kleine randomisierte Studien und Registerdaten deuten darauf hin, dass die IABP bei akutem Herzversagen, insbesondere als Überbrückung zur Herztransplantation oder LVAD-Implantation, hämodynamische Stabilität bieten kann. Retrospektive Analysen zeigen, dass die IABP das klinische Risikoprofil senken könnte, ohne die Letalität oder Komplikationsrate signifikant zu erhöhen [20–24].
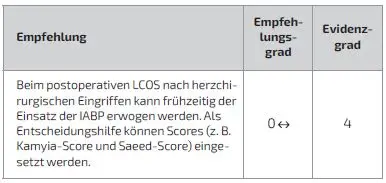
Schlüsselfrage 6: Soll die IABP bei postoperativem low cardiac output syndrome (LCOS) nach herzchirurgischen Eingriffen eingesetzt werden?
Im Bereich der Kardiochirurgie stellt der postoperative Einsatz der IABP im Rahmen der Behandlung eines therapierefraktären LCOS eine klassische Indikation dar: Die Rationale der IABP-Therapie in diesem Kontext ist, dass im Rahmen des LCOS reduzierte HZV anzuheben und zu normalisieren. Retrospektive Analysen zeigen, dass die IABP bei hämodynamisch instabilen Patienten eingesetzt wird, wobei die Mortalität hoch bleibt, insbesondere bei schwerer linksventrikulärer Dysfunktion. Ein optimaler Implantationszeitpunkt ist unklar, jedoch wird ein früher Einsatz empfohlen, wenn trotz kausaler Therapie weiterhin hohe Dosen von Vasopressoren oder Inotropika erforderlich sind. Ein neu entwickelter IABP-Score könnte helfen, Patienten mit einer hohen Erfolgswahrscheinlichkeit für die IABP-Therapie zu identifizieren und in ungünstigen Fällen frühzeitig alternative Kreislaufunterstützungs- verfahren in Betracht zu ziehen [25–29].
Die IABP als prophylaktisches Unterstützungsverfahren
Schlüsselfrage 7: Soll die IABP prophylaktisch bei Hochrisikopatienten vor herzchirurgischen Eingriffen eingesetzt werden?
Der prophylaktische Einsatz der IABP wird seit vielen Jahren diskutiert. Die Rationale besteht in einer intendierten hämodynamischen Stabilisierung in der perioperativen Phase. Der prophylaktische Einsatz der IABP bei kardiochirurgischen Risikopatienten wurde bislang in 11 monozentrischen RCTs an mehr als 1100 Patienten untersucht. Eine Meta-Analyse von Rocha Ferreira et al. (2018) zeigte eine signifikante Reduktion der Mortalität, wobei bei isolierter Betrachtung neuerer Studien der positive Effekt nicht mehr nachweisbar war. Andere Meta-Analysen, die auch Beobachtungsstudien einbezogen, bestätigten ebenfalls eine Mortalitätsreduktion durch den prophylaktischen Einsatz der IABP bei Hochrisikopatienten. Die vorliegenden Daten und die Abwägung der Risiken ohne adäquate Alternativen sprechen dafür, den prophylaktischen Einsatz der IABP bei Hochrisikopatienten zu empfehlen. Eine US-amerikanische Expertenempfehlung der American Association for Thoracic Surgery (AATS) unterstützt dies, wenn auch mit einem etwas niedrigeren Empfehlungsgrad. Diese Empfehlung spricht den Einsatz der IABP bei Patienten mit chronischer oder dekompensierter Herzinsuffizienz, fortgeschrittenem linken Ventrikelumbau oder Anzeichen einer Organfunktionsstörung aus [30–53].
Schlüsselfrage 8: Was sind geeignete Kriterien für Hochrisikopatienten, die von einer prophylaktischen IABP-Implantation profitieren?
Die in den Studien zum prophylaktischen Einsatz der IABP genutzten Einschlusskriterien sind heterogen (z. B. eine relevante HSS oder einen moderat erhöhten EuroSCORE). Die Leitliniengruppe möchte eine Definition zur Verfügung stellen, die nach Expertenkonsens und Überblick über die Studienlage eine geeignete Eingrenzung von Patienten erlaubt, die von einer prophylaktischen IABP-Anlage profitieren.
Schlüsselfrage 9: Soll die IABP während der extrakorporpalen Zirkulation zur Erzeugung eines pulsatilen Flusses eingesetzt werden?
Seit der Einführung der Herz-Lungen-Maschine beschäftigten sich viele Arbeitsgruppen mit der Fragestellung, ob ein pulsatiler Fluss einem nicht-pulsatilen Fluss überlegen ist. Wesolowski beschäftigte sich als einer der ersten Forscher in den 1950er Jahren mit dieser Thematik. Seine Ergebnisse zeigten keinen eindeutigen Unterschied zwischen der pulsatilen und der nicht-pulsatilen Perfusion [54]. Aufgrund seiner initialen Ergebnisse und des technisch einfacheren und weniger störanfälligen Pumpensystems setzte sich die nicht-pulsatile Perfusion durch. Mehrere RCTs und tierexperimentelle Daten zeigen einen positiven Effekt der pulsatilen Perfusion auf die postoperativen Organfunktionen [41,55–87].
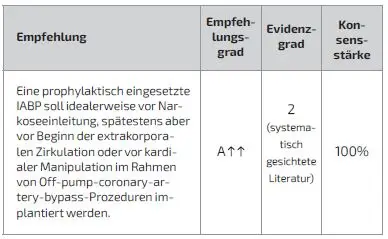
Schlüsselfrage 10: Wann soll die IABP prophylaktisch implantiert werden?
Für die prophylaktische IABP-Implantation ergibt sich die Frage nach dem optimalen Zeitpunkt. Hierbei muss abgewogen werden zwischen einer möglichst kurzen Zeitspanne präoperativ, um IABP-assoziierte Komplikationsraten möglichst niedrig zu halten, und einer Zeitspanne, die lang genug ist, um die präkonditionierenden und stabilisierenden Effekte der IABP bestmöglich zu entfalten [34,37,88].
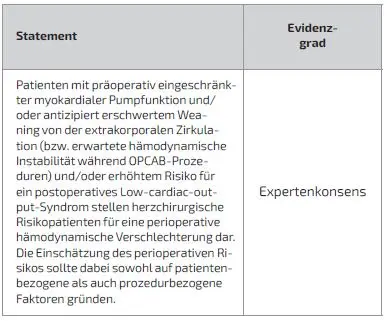
Schlüsselfrage 11: Unter welchen Voraussetzungen soll die IABP zur Unterstützung des HLM-Abgangs eingesetzt werden?
Bei erschwerter Entwöhnung eines Patienten von der extrakorporalen Zirkulation könnte der Einsatz der IABP die Stabilität und Entwöhnung des Patienten erleichtern. Ein erschwertes Weaning von der Herz-Lungen-Maschine ist mit einer erhöhten Mortalität und Morbidität verbunden, wobei der Einsatz einer IABP den Weaning-Prozess erleichtern und die Prognose verbessern kann. Verschiedene Studien zeigen, dass die IABP in vielen Fällen erfolgreich beim Weaning-Versagen hilft, allerdings ist die Mortalität der Patienten trotz IABP relativ hoch. Eine vergleichende Studie zeigte keine signifikanten Unterschiede in der Mortalität zwischen Patienten mit erfolgreicher oder frustraner IABP-Anlage, jedoch eine niedrigere Mortalität bei frühzeitiger Implantation. Es wird empfohlen, bei erwartetem Weaning-Versagen mit der IABP zu beginnen, da sie weniger invasiv ist und ein späterer Übergang zu einem ECLS unter optimierten Bedingungen erfolgen kann [25,89–98].
Management der IABP
Schlüsselfrage 12: Welche Zugangswege zur IABP-Implantation stehen zur Verfügung und sollen genutzt werden?
Zur Implantation einer IABP stehen verschiedene Zugangswege zur Verfügung. In den vergangenen Jahren ist eine Zunahme an Publikationen und Implantationstechniken zur axillären Implantation der IABP zu verzeichnen, die unter anderem im Rahmen einer Bridge-to-transplant-Situation bei Patienten mit schwerer Herzinsuffizienz eingesetzt werden [99–106].
Schlüsselfrage 13: Soll die IABP mit oder ohne Schleuse implantiert werden?
Die IABP-Systeme ermöglichen die Implantation unter Verwendung einer Gefäßschleuse sowie zunehmend seit Beginn der 2000er Jahre auch eine schleusenlose Einlage in die arteriellen Gefäße. Verschiedene Registerdaten zeigen eine geringere Rate an Blutungs- und ischämischen Komplikationen bei schleusenloser Anlage [107–114].
Schlüsselfrage 14: Wie soll die Ballongröße gewählt werden?
IABP-Systeme verschiedener Hersteller stehen zur Anwendung der intraaortalen Gegenpulsation in Deutschland mit verschiedenen Ballongößen (30 ml bis 50 ml) zur Verfügung. Dem Grundprinzip der intraaortalen Gegenpulsation folgend, korreliert die Unterstützungsleistung mit dem Ballonvolumen und damit dem potenziell verdrängten Blutvolumen in der Aorta [115–119].
Schlüsselfrage 15: Was sind Zielparameter einer erfolgreichen IABP-Therapie?
Zielparameter der IABP-Therapie könnten hilfreich sein, um den Effekt einer IABP-Therapie zu objektivieren und damit zu erkennen, ob die IABP einen ausreichenden Effekt erzielt oder ob eine Eskalation zu einer invasiveren Form der mechanischen Kreislaufunterstützung erforderlich ist [18,27,90,95– 97,120–123].
Schlüsselfrage 16: Welches Monitoring soll während der IABP-Therapie durchgeführt werden?
Patienten mit einliegender IABP müssen nicht nur aufgrund ihrer häufig bestehenden hämodynamischen Instabilität, sondern auch aufgrund möglicher spezifischer systembedingter Komplikationen intensivmedizinisch überwacht werden. Zur Thematik des Basis- bzw. erweiterten hämodynamischen Monitorings wird an dieser Stelle auf die Leitlinie „Intensivmedizinische Versorgung herzchirurgischer Patienten – hämodynamisches Monitoring und Herz-Kreislauf-Therapie“ verwiesen [122].
Schlüsselfrage 17: Wie sollte die Blutgerinnung während IABP-Therapie gesteuert werden?
Die IABP als intravasaler Fremdkörper bildet grundsätzlich ein Risiko für Thrombenbildung. Studien aus den letzten Jahrzehnten zeigen eine deutliche Reduktion ischämischer Komplikationen unter IABP-Therapie, was vor allem auf kleinere Katheter zurückgeführt wird. Eine universelle Heparinisierung unter IABP-Therapie erhöht das Blutungsrisiko signifikant, ohne eine klare Verringerung thrombembolischer Komplikationen zu bewirken. Eine selektive Antikoagulation scheint dagegen sicher, insbesondere wenn sie auf bestehende Indikationen wie akutes Koronarsyndrom abgestimmt wird. Die Interpretation großer Registerstudien bleibt schwierig, da viele Einflussfaktoren wie Blutdruck oder Anwendungsdauer nicht ausreichend berücksichtigt wurden. Daher wird keine generelle Antikoagulation unter IABP-Therapie empfohlen, sondern eine individuelle Entscheidung anhand der Begleiterkrankungen des Patienten bevorzugt [111,124–126].
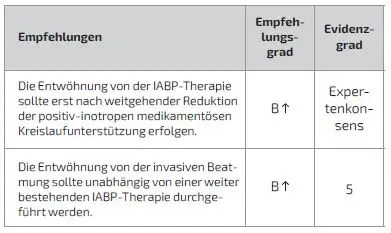
Entwöhnung von der IABP
Ohne wissenschaftliche Evidenz wird seit der klinischen Einführung der IABP eine schrittweise Entwöhnung der IABP vor deren Entfernung propagiert und in den meisten kardiochirurgischen Kliniken auch durchgeführt [4]. Dabei stehen dem Kliniker zwei Verfahren der Entwöhnung zur Verfügung, die auch miteinander kombiniert werden können: Zum einen die schrittweise Reduktion der Unterstützungsfrequenz von 1:1, d. h. jeder Herzschlag wird durch die IABP augmentiert, auf 1:2 (jeder zweite Herzschlag wird augmentiert) bis hin zu 1:8 (Frequenzreduktion). Alternativ kann das Ballonvolumen stufenweise in Schritten von 10 % reduziert werden (Volumenreduktion). In diesem Zusammenhang stellen sich drei Schlüsselfragen:
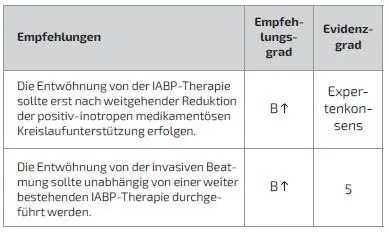
Schlüsselfrage 18: Ist ein stufenweises Weaning der IABP generell sinnvoll?
Schlüsselfrage 19: Wann sollte das Weaning eingeleitet bzw. welche Parameter sollten als Prädiktoren für ein erfolgreiches Weaning herangezogen werden?
Schlüsselfrage 20: Welches Weaning-Verfahren (Frequenzreduktion versus Volumenreduktion) ist zu bevorzugen?
Schlüsselfrage 21: Wie lange sollte die IABP maximal angewandt werden?
Insbesondere in der Frühphase der IABP-Nutzung sorgte eine hohe Inzidenz von IABP-assoziierten Komplikationen nicht nur zu einer eher zurückhaltenden Indikationsstellung, sondern auch zu der Auffassung, eine längerfristig durchgeführte IABP-Therapie führe zu einer signifikant gesteigerten Rate schwerer Komplikationen [112,127–136].
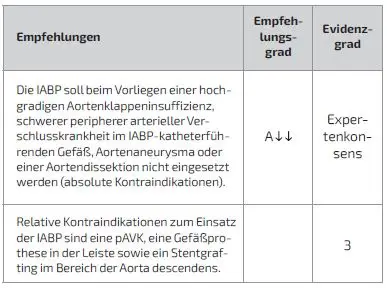
Schlüsselfrage 22: Was sind Kontraindikationen der IABP-Therapie?
Aus pathophysiologischen Abwägungen und klinischen Erfahrungen zeigt sich, dass Umstände existieren, unter denen die IABP-Therapie nicht durchgeführt werden sollte (absolute Kontraindikationen) bzw. unter denen die Risiken gegenüber dem potenziellen Nutzen erhöht sind (relative Kontraindikationen) [17,100,107,136–148].
Welche pflegerischen Maßnahmen sind in der Betreuung von IABP-Patienten relevant?
Erstmals wurden in dieser Leitlinienarbeit pflegerisch relevante Aspekte im Umgang mit Patienten, die mit IABP therapiert werden, eingearbeitet.
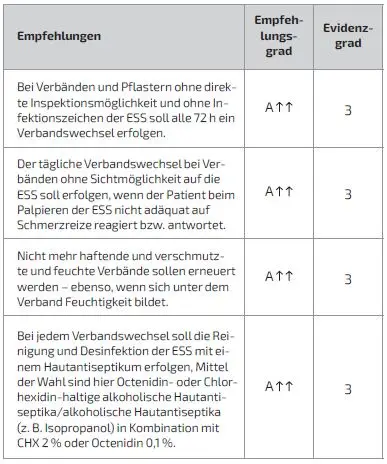
Schlüsselfrage 23: Wie soll die Punktionsstelle des arteriellen Katheters bei Patienten mit liegender intraaortaler Ballonpumpe versorgt werden?
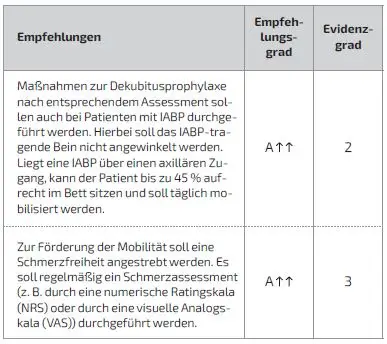
Schlüsselfrage 24: Wie soll die Lagerung bzw. Mobilisation und Dekubitusprävention von Patienten mit liegender intraaortaler Ballonpumpe erfolgen?
Die IABP im Kontext weiterer mechanischer Kreislaufunterstützungsverfahren
Schlüsselfrage 25: Wie soll die Differentialindikation zur IABP-Implantation versus anderen mechanischen Kreis- laufunterstützungsverfahren (MCS) gestellt werden?
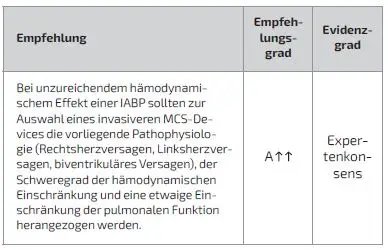
Die Auswahl eines der klinischen Situation angemessenen mechanischen Kreislaufunterstützungsverfahrens (MCS) sollte nach möglichst objektiven Kriterien erfolgen, eine bedarfsgerechte hämodynamische Unterstützung ermöglichen und Komplikationen vermeiden. Die IABP zeichnet sich durch eine im Vergleich zu invasiveren MCS geringere Komplikationsrate aus, erzielt aber auch einen weniger ausgeprägten hämodynamischen Effekt. Bei der Auswahl eines MCS findet in der Regel eine Abwägung zwischen erforderlicher Intensität der hämodynamischen Unterstützung und der Risiken statt, die durch die Invasivität des Verfahrens entstehen. Zudem spielen zeitlich-logistische Aspekte und die lokale Verfügbarkeit und Erfahrungen von/mit unterschiedlichen MCS-Systemen eine Rolle.
Schlüsselfrage 26: Soll die IABP in Kombination mit anderen mechanischen Kreislaufunterstützungsverfahren ein- gesetzt werden?
Die IABP kann durch ihre nachlastsenkenden Effekte im Kontext einer aktiven mechanischen Kreislaufunterstützung die Entlastung des linken Ventrikels unterstützen [149–151].
Die IABP bei Kindern und Jugendlichen
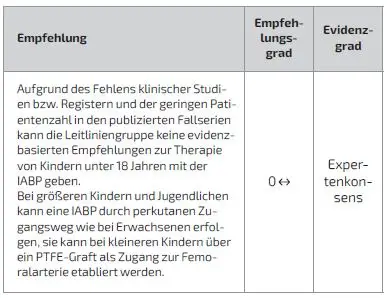
Schlüsselfrage 27: Sollte die IABP bei Kindern und Jugendlichen eingesetzt werden?
Die Optionen für kurzfristigen MCS sind bei Kindern aufgrund der Größenverhältnisse insbesondere bei Neugeborenen und Säuglingen im Wesentlichen auf ECMO-/ECLS-Systeme beschränkt. Bei größeren Kindern, die sich somatisch den Erwachsenen annähern, wären auch intravaskulär zugeführte MCS wie die IABP oder die Impella-Pumpen vorstellbar. In der durch die Leitliniengruppe durchgeführten Umfrage unter den herzchirurgischen Kliniken in Deutschland gab keine der Kliniken an, die IABP bei Patienten unter 18 Jahren zu nutzen.
Das Literaturverzeichnis findet sich aufgrund seines Umfangs im digitalen Supplement zu diesem Artikel.