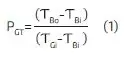Einleitung
Die Oxygenierung des venösen Patientenblutes wird im Rahmen der extrakorporalen Zirkulation mit Hilfe des Oxygenators durchgeführt. Mit dem Funktionsprinzip der Lunge als Vorbild werden in standardmäßig eingesetzten Membranoxygenatoren Gas und Blut durch semipermeable Membranhohlfasern (Kapillare) voneinander getrennt [1]. Der Übertritt der Atemgase auf die jeweilige Blutbeziehungsweise Gasseite wird durch die Partialdrücke entlang des Konzentrationsgefälles der Gase bestimmt. Bei dem Perfusionsgas (Frischgas) handelt es sich um ein einstellbares Gasgemisch aus Luft und Sauerstoff (O2). Das Frischgasgemisch tritt über einen Gaseinlass-Port in den Oxygenator ein und durchströmt die Kapillare in möglichst gegenläufiger Richtung zum Blutstrom. Der Gastransfer erfolgt über die Mikroporen besetzte Membranoberfläche aufgrund von freier Diffusion entlang des Partialdruckgradienten [1,2]. Für die vorliegende Studie wird postuliert, dass mit dem Gasübertritt entlang der Kapillare zeitgleich ein Wärmeaustausch erfolgt. Während der extrakorporalen Zirkulation ist eine gezielte Temperaturregulation der Patienten erforderlich, wobei besonders das Herabsetzen der Körperkerntemperatur eine signifikante Rolle spielt. Die Hypothermie-bedingte Reduktion des O2-Bedarfs im Gewebe ermöglicht intraoperativ eine adäquate Perfusion bei niedrigeren Blutflüssen [3]. Die Regulation der Patientenbluttemperatur erfolgt standardmäßig mittels eines Hypothermiegerätes. Hierbei zirkuliert eine temperierte Kühlflüssigkeit durch ein separates Trennsystem (Wärmetauscher) innerhalb des Oxygenators. Der Wärmetauscher ist in den meisten handelsüblichen Oxygenator-Modellen aus zentral angeordneten Rohrbündeln aufgebaut [1]. Kammerkonfigurationen, bei der die Kühlflüssigkeit und das Blut im Oxygenator möglichst im Gegen- oder Kreuzstrom aneinander vorbeigeführt werden, sind mit einem effizienten Wärmeübergang assoziiert [4]. Im Rahmen der Oxygenator-Entwicklung sollen Möglichkeiten zur Temperierung des Patientenblutes ohne die Verwendung eines externen Hypothermiegerätes evaluiert werden. Um die Datengrundlage hierfür zu erweitern, wird anhand der vorliegenden Studie die Wärmeübertragung an der Hohlfasermembran betrachtet. Die erhobenen Leistungsdaten werden im Rahmen einer umfassenden statistischen Analyse dargelegt.
Material und Methoden
Die experimentelle In-vitro-Studie wurde im Zeitraum von Oktober 2023 bis März 2024 am Lehrstuhl für Strömungsmechanik der Friedrich-Alexander-Universität (FAU) Erlangen-Nürnberg in Kooperation mit der Perfusiologie der herzchirurgischen Klinik des Universitätsklinikums Erlangen durchgeführt. Im Rahmen des Studiendesigns wurden verschiedene Einflussfaktoren auf die Wärmeübertragung an der Hohlfasermembran getestet. Hierbei handelt es sich um den Einfluss der Frischgastemperatur, der FiO2-Konzentration des Frischgases, der Blutflussrate im Testkreislauf sowie verschiedener Kammerkonfigurationen unterschiedlicher Oxygenator-Modelle.
Versuchsaufbau
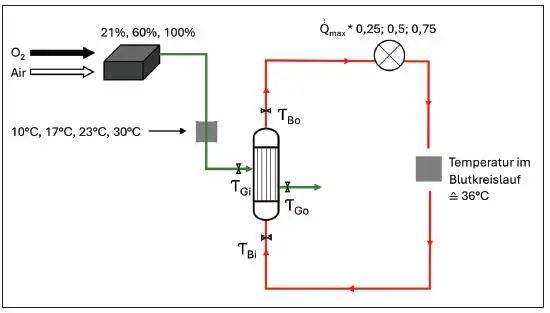
Vier verschiedene Test-Oxygenatoren (Affinity Fusion, Medtronic; Inspire 7M, Sorin; Capiox NX19, Terumo; D100 Physio+, Kids, Sorin) wurden entsprechend der Abbildung 1 in einen einfachen Kreislauf integriert und die Temperatur mit Hilfe eines Laborkühlgerätes (Thermo Haake, Erlangen, Deutschland; C41P) auf 36,7 ± 0,5 °C konstant gehalten. Gemessen wurden jeweils 25 %, 50 % und 75 % der maximalen blutseitigen Durchflussrate (Q̇max) der Test-Oxygenatoren und der erzeugte Volumenstrom Q̇B wurde mit Hilfe eines Flussmessgerätes kontrolliert. Der O2-Anteil des im Gasblender gemischten Gases wurde bei 21 %, 60 % und 100 % FiO2 erfasst. Der Einfluss der Gastemperatur wird bei vier definierten Temperaturen (10 °C, 17 °C, 23 °C, 30 °C) gemessen, wobei der Gasfluss konstant auf 5 l/min gehalten wird.
Am Blutein- (B,i ) und Blutauslass (B,o ) sowie am Gasein- (G,i ) und Gasauslass (G,o ) der Test-Oxygenatoren wurden Temperatursensoren aufgebracht. Zur kontinuierlichen digitalen Temperaturerfassung wurden Temperatursonden an den Ein- und Auslässen der Gas- und Blutseite auf einen Mikrocontroller (Arduino, Somerville, MA, USA) montiert.
Die definierten Parametereinstellungen der Einflussfaktoren (Gastemperatur, FiO2-Konzentration, Blutflussgeschwindigkeit, Oxygenator-Modell) wurden in jeder möglichen Konstellation kombiniert. Für jede Parameterkombination wurde eine Messreihe in einem Messintervall von 5 Minuten aufgenommen, wobei pro Sekunde zwei Messungen dokumentiert wurden. Zum Ausschluss von Zufallsmessungen und zur statistischen Beurteilung wurden Daten zu allen Parameterkominationen mit einer Anzahl von drei Wiederholungen erhoben.
Leistungsberechnung
Analog zu den Leistungsangaben eines handelsüblichen Wärmetauschers soll die Wärmeübertragung an der Oxygenierungseinheit (Hohlfasermembran) anhand von Performance- beziehungsweise Leistungsfaktoren (P) in Werten zwischen 0 und 1 angegeben werden. Die Formel für den Leistungsfaktor des Gastauschers (PGT ) ergibt sich aus dem Quotienten der Temperaturdifferenz zwischen dem Blutauslass (Bo ) und Bluteinlass (Bi ) und dem Gas- (Gi ) und dem Bluteinlass (Bi ):
Statistisches Design
Die statistische Auswertung erfolgte mit Hilfe der Statistiksoftware R (Version 4.4.0) [5]. Die Daten wurden zunächst in einer zusammenfassenden Tabelle gesammelt, die die Basis der Analyse darstellt. Für das Einlesen der Daten sowie die graphische Darstellung der Ergebnisse wurden die (Erweiterungs-)Pakete openxlsx und ggplot2 [6,7] verwendet.
Die Analyse basiert auf der Forschungshypothese, dass die Gastemperatur des Perfusionsgases im Rahmen der Wärmeübertragung an der Hohlfasermembran die Temperatur des Patientenblutes beeinflusst. Das Signifikanzniveau wurde für alle statistischen Tests auf = 0,05 festgelegt.
Für die Auswahl geeigneter Tests wurden zunächst die Verteilung der Daten, die Anzahl und die Abhängigkeiten der Gruppen (Variablen) berücksichtigt und diese anschließend in unabhängige (Prädiktoren) und abhängige (Kriterien) Variablen gegliedert. Zu den abhängigen Variablen gehören die Mittelwerte der gemessenen Temperaturen aus einer 5-minütigen Messreihe an den verschiedenen Messstellen (Gi, Go, Bi, Bo) sowie die errechneten Leistungsfaktoren für die Oxygenierungseinheit (PGB). Hieraus ergaben sich fünf verschiedene Kriterien, die mit y1-5 gekennzeichnet wurden. Als unabhängige Variablen (x1-4) gelten die vier oben genannten Einflussfaktoren (Frischgastemperatur, FiO2-Konzentration, Blutflussrate, Test-Oxygenator).
Im nächsten Schritt wurden geeignete multiple lineare Modelle mit gemischten Effekten für die Analyse erarbeitet, wobei für den vorliegenden Datensatz die unabhängigen Variablen beispielhaft in Zusammenhang mit der abhängigen Variable Gi (y1) gebracht werden (Formel 2). Das Modell wird analog für jede weitere abhängige Variable angewendet.
Dabei handelt es sich bei den Variablen Gastemperatur, FiO2, Blutflussrate und Oxygenator-Modell um sogenannte feste Effekte.
Da sich die leicht veränderten Versuchsbedingungen der verschiedenen Versuchstage für jedes Modell etwas unterschiedlich auf die Ergebnisse auswirken könnten, sollen durch das Miteinbeziehen des Versuchsdatums als „random effect“ Auffälligkeiten in den diagnostischen Plots reduziert werden. Der Ausdruck (Modell | Datum) spezifiziert den zufälligen Effekt für die Variable „Datum“, wobei für jedes Modell ein separater „random intercept“ ermittelt wird. Dies erlaubt es, mögliche Unterschiede in den Ausgangswerten sowie in den Einflussstärken der Prädiktoren zwischen den einzelnen Test-Oxygenatoren zu erfassen.
Die Gültigkeit und Güte der linearen Mixed-effects-Modelle werden in der Analyse mit Hilfe der Funktion „check_model“ aus dem Paket „performance“ [8] bestimmt. Zusätzlich wurde mit Hilfe von „qqplots“ die Normalverteilung der Residuen überprüft [9].
Im Rahmen der Modellbewertung und -verbesserung erfolgten über die Funktion „summary“ aus dem (Grund-)Paket „base“ [5] unter anderem Angaben zu den geschätzten Regressionskoeffizienten. Ein kleiner p-Wert (p < 0,05) der Koeffizienten weist hierbei auf einen Einfluss des Prädiktors auf das Kriterium hin.
Für das weitere Vorgehen steht die Abweichung der verschiedenen Gruppenmittelwerte der getesteten (unabhängigen) Variablen im Fokus der Betrachtung. Hierfür wird die Varianzanalyse (ANOVA – Analysis of Variance) herangezogen. Bei der ANOVA wird der Einfluss von einem oder mehreren Faktoren auf das Ergebnis untersucht, wobei auf bestimmte Kovariablen adjustiert wird [9]. Basierend auf dem beschriebenen Modell wird eine lineare ANOVA mit gemischten Effekten durchgeführt und diese für die genannten unabhängigen Variablen dargestellt. Da der statistische Test in der ANOVA lediglich angibt, ob mindestens eine der Gruppen von den anderen signifikant abweicht, können Post-hoc-Tests dabei helfen, Gruppenunterschiede spezifischer herauszuarbeiten [10]. Hierfür wurden im Rahmen der Analyse verschiedene Pakete verwendet. Mit Funktionen aus dem Paket „estimated marginal means“ (emmeans) [11] können Paarvergleiche der geschätzten marginalen Mittelwerte und deren Konfidenzintervalle für verschiedene kategoriale Variablen der Modelle durchgeführt werden. Alternativ ist die Funktion „general linear hypothesis test“ (glht) aus dem Paket „multcomp“ [12] eine Methode zur Überprüfung von spezifischen linearen Kontrasten zwischen den Gruppen. Im Fall der vorliegenden Daten wird der sogenannte Tukey-Test verwendet, um zusätzlich das multiple Testen zu berücksichtigen, welches durch die multiplen Post-hoc-Tests entsteht.
Ergebnisse
Im Folgenden werden die wichtigsten Aspekte der Auswertung dargestellt und näher betrachtet. Eine umfassende Darstellung der statistischen Analyse ist im digitalen Supplement aufgeführt:
Ergebnisse der ANOVA-Analysen
Im Rahmen der ANOVA wird der Einfluss der im Modell verwendeten Prädiktoren (Gastemperatur, FiO₂, Blutflussrate, Modell) auf die verschiedenen Kriterien untersucht. Für das Kriterium „Gaseinlass“ (Gi) ergibt sich für den Prädiktor „Gastemperatur“ ein p-Wert von <0,001. Für das Kriterium „Gasauslass“ (Go) liegen die p-Werte für das Oxygenator-Modell und die Blutflussrate ebenfalls unter 0,001. Zusätzlich zeigt sich für das FiO₂ im Zusammenhang mit der Temperatur am Gasauslass ein p-Wert von <0,05. Die Gastemperatur weist hier keinen statistisch signifikanten Einfluss auf. Am Bluteinlass (Bi) ergeben sich für das Oxygenator-Modell, die FiO₂-Konzentration und die Blutflussrate p-Werte <0,001. Die Gastemperatur zeigt hier einen p-Wert <0,01. Beim Blutauslass (Bo) zeigen alle einbezogenen Prädiktoren p-Werte <0,001.
Einfluss der verschiedenen Prädiktoren auf die Wärmeübertragung
Der Einfluss der verschiedenen Prädiktoren (Frischgastemperatur, FiO2-Konzentration, Blutflussrate, Test-Oxygenator) auf die Wärmeübertragung wird anhand von Box- und Whisker-plots dargestellt (Abb. 2 a–d).
In Abbildung 2 a sind die Leistungsfaktoren in Bezug auf den Einfluss der Gastemperatur zusammengefasst, wobei bei Einstellungen mit einer Gastemperatur von 30 °C Leistungsfaktoren von -0,009 (-0,9 %) bis zu 0,181 (18,1 %) erzielt werden. In Abbildung 2 b sind die Leistungsfaktoren in Abhängigkeit des FiO2-Anteils aufgezeigt. Die Werte bei einem FiO2 von 21 % liegen in einem Wertebereich von 0,006 (0,6 %) bis 0,11 (11 %). Die Leistungsfaktoren der beiden anderen FiO2– Konzentrationen liegen für beide in einem Bereich zwischen 0,014 (1,4 %) und 0,135 (13,5 %), wobei der Median der Konzentration FiO2 = 60 % geringfügig höher liegt als der bei einem FiO2 von 100 %.
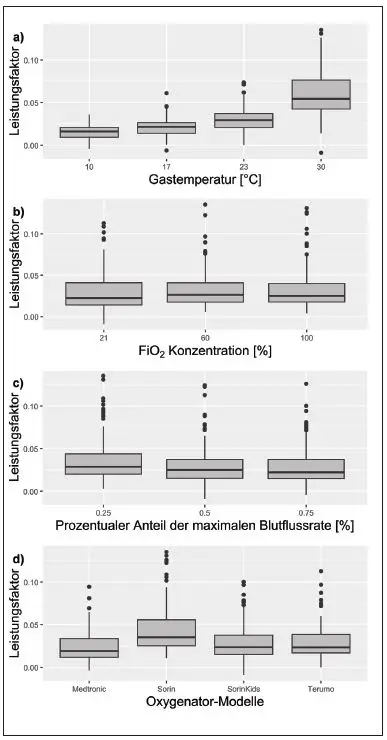
In Abbildung 2 c ist der Einfluss der Blutflussrate auf die Leistungsfaktoren dargestellt. Aus den Einstellungsmöglichkeiten innerhalb des Prädiktors „Blutflussrate“ werden die höchsten Leistungsfaktoren bei der geringsten Blutflussrate von 25 % der maximalen Durchflussrate, in einem Bereich zwischen 0,006 (0,6 %) und 0,135 (13,5 %) erzielt.
In Abbildung 2 d wurde der Einfluss des Oxygenator-Modells erfasst. Berechnete Leistungsfaktoren der drei Modelle von Medtronic, Sorin Kids und Terumo weisen insgesamt ähnliche Werte von bis zu 0,113 (11,3 %) auf. Das Modell der Firma Sorin erzielt mit Leistungsfaktoren von bis zu 0,231 (23,1 %) Werte in einem höheren Bereich.
Diskussion
Die Wärmeübertragung an der Hohlfasermembran konnte in der vorliegenden experimentellen Studie spezifiziert und über errechnete Leistungsfaktoren quantifiziert werden. Die Forschungshypothese (H1) kann aufgrund des Einflusses der Perfusionsgastemperatur auf die Patientenbluttemperatur bestätigt werden.
Einfluss der Gastemperatur
Der Graphik aus Abbildung 2 a ist zu entnehmen, dass die verschiedenen Einstellungen der Test-Temperaturen des Frischgases unterschiedliche Leistungsfaktoren erzielen. Höhere Gastemperaturen am Oxygenator-Eingang gehen hierbei mit einer gesteigerten Wärmeübertragung an der Membran einher. Eine Erklärung dafür bietet sowohl die eingestellte Temperatur im Blutkreislauf (36,7 ± 0,5 °C) als auch die Art, wie die verschiedenen Messwerte in die Berechnung des Leistungsfaktors mit einfließen.
Aufgrund der unterschiedlichen Temperaturen der beiden Medien Gas und Blut besteht an der Membran eine Tendenz zum Temperaturangleich. Basierend auf dem zweiten Hauptsatz der Thermodynamik ist der erforderliche Wärmebetrag zum Temperaturangleich höher, je weiter die Temperaturen der beiden Medien auseinanderliegen, da Wärme in die Richtung des Temperaturgefälles strömt [13]. Hieraus kann geschlossen werden, dass der Leistungsfaktor des Gastauschers maßgeblich von dem Verhältnis zwischen der Gastemperatur am Oxygenator-Eingang und der Bluttemperatur abhängig ist.
Dieser Effekt zeigt sich weiterhin in den Ergebnissen der ANOVA (siehe digitales Supplement). Aus dem Zusammenhang der beiden Ausgaben zum ² (Chi square) und den Freiheitsgraden (Anzahl frei veränderbarer Werte, ohne die Änderung eines betrachteten Parameters) errechnet sich die Interaktion zwischen den abhängigen und den unabhängigen Variablen, was anhand des Pr(>²) angegeben wird [10]. Die Ergebnisse der ANOVA für die Messstelle Gaseinlass zeigt für den Prädiktor „Gastemperatur“ eine Signifikanz auf, was den Einfluss der Gastemperatur auf die Wärmeübertragung an der Hohlfasermembran bestätigt.
Abbildung 2 a zeigt, dass die berechneten Leistungsfaktoren zwar überwiegend im positiven Bereich liegen, dennoch vereinzelt auch negative Werte auftreten. Dies weist darauf hin, dass in diesen Fällen die Wärmeübertragung nicht von der Gas- auf die Blutseite, sondern ausschließlich umgekehrt erfolgt.
In Bezug auf den Einfluss der Frischgastemperatur kann zusammenfassend ausgesagt werden, dass eine Wärmeübertragung an der Hohlfasermembran zwar nachweisbar ist, jedoch erwartungsgemäß niedrig ausfällt. Es handelt sich um Werte, mit großer Diskrepanz zur standardmäßig erbrachten Leistung der Wärmetauschereinheit, die einen akzeptablen Wärmeaustausch ab Leistungsfaktoren von 0,5 (50 %) vorsieht.
Einfluss der FiO2-Konzentration
Aufgrund der geringfügig höheren Wärmeleitfähigkeit von Sauerstoff ( = 26,0 *10-3 W/mK) gegenüber der von Luft ( = 25,87 *10-3 W/mK), wären bei Gaseinstellungen mit einem niedrigeren FiO2-Gehalt entsprechend niedrigere Leistungsfaktoren zu erwarten [13].
Anhand der Ergebnisse in Abbildung 2 b ist zu erkennen, dass die Leistungsfaktoren der Luft-Messung insgesamt geringer ausfallen als die der beiden anderen FiO2-Konzentrationen. Jedoch handelt es sich um nur sehr geringfügige Unterschiede, sodass die Herkunft der Abweichungen ebenfalls in an- deren Einflussfaktoren, wie beispielsweise leichten Temperaturabweichungen der Gase (Luft und O2) begründet liegen könnten.
Auf einen direkten Zusammenhang zwischen der FiO2-Konzentration und der Wärmeübertragung an der Hohlfasermembran kann daher nicht geschlossen werden.
Einfluss der Blutflussrate
In Bezug auf die Blutflussrate stellen niedrige Blutflüsse in Kombination mit hohen Gasflüssen zunächst günstige Bedingungen für den Gastransfer an der Hohlfasermembran dar [14]. Unter der Annahme, dass dies ebenfalls für die Wärmeübertragung gilt, stellt in der vorliegenden Studie die Parametereinstellung mit einem Blutfluss von 0,25*Q̇max bei einem konstanten Gasfluss von 5 l/min die besten Voraussetzungen für den Blutfluss dar [14,15]. Die Leistungsfaktoren müssten demnach mit steigender Blutflussrate insgesamt absinken. Allerdings sind zwischen den Leistungsfaktoren der Blutflussraten von 0,5*Q̇max und 0,75*Q̇max in der Abbildung 2 c kaum Unterschiede festzustellen.
Eine mögliche Begründung hierfür liefert die konstante Einstellung der Gasflussgeschwindigkeit. Je höher die Blutflussgeschwindigkeit bei gleichbleibendem Gasfluss, desto weiter entfernt sich das Verhältnis zwischen Blut- und Gasfluss von den optimalen Bedingungen, was sich in den Ergebnissen in geringeren Leistungsfaktoren äußert.
Einfluss der verschiedenen Oxygenator-Modelle
Die Bauart eines Oxygenators spielt ebenfalls eine Rolle bei der Wärmeübertragung an der Gasaustauschfläche. In Abbildung 2 d ist dargestellt, dass die drei Modelle Affinity Fusion von Medtronic, Capiox NX19 von Terumo sowie D100 Physio+, Kids von Sorin vergleichbare Leistungsfaktoren erzielen, wobei für das Modell Inspire 7M von Sorin höhere Werte ausgegeben werden. Für die gesteigerte Performance des zuletzt genannten Modells bietet die Konfiguration der Kompartimente im Oxygenator einen möglichen Erklärungsansatz. Die einzelnen Kompartimente sind hier, anders als bei den anderen getesteten Modellen, klarer voneinander getrennt, was in einer kontrollierten Strömungsführung innerhalb des Oxygenators resultiert [4]. Das Blut passiert die Gasaustauschfläche sowie den Wärmetauscher im Gegenstrom, was mit einem erhöhten Stofftransfer einhergeht.
Bei dem Vergleich der Box- und Whiskerplots der übrigen drei Modelle ist zu erkennen, dass die Größe der Boxen überwiegend übereinstimmt und die Mediane auf vergleichbarer Höhe liegen. Zu nennen ist, dass die Whiskerplots des Modells von Terumo am kürzesten und die Boxplots (Interquartilsabstand) geringfügig kleiner sind als die der beiden anderen Oxygenator-Typen. Eine Interpretation dieses Effekts ist, dass dieses Modell robuster gegenüber den Einflüssen der anderen Prädiktoren ist, was sich anhand von konstanteren Leistungsfaktoren zeigt.
Klinische Relevanz
In Bezug auf die gebrauchsübliche klinische Anwendung findet die Temperierung des Patientenblutes maßgeblich über die Wärmetauscher-Einheit im Oxygenator-System statt. Die durch die Frischgastemperatur beeinflusste Wärmeübertragung an der Hohlfasermembran spielt hierbei nur eine untergeordnete Rolle.
Vor dem Hintergrund der Oxygenator-Entwicklung wird im Rahmen der Studie in Betracht gezogen, dass Hypothermiegeräte in der klinischen Praxis einige Nachteile mit sich bringen. Infektionen mit dem Mycobakterium chimaera nach herzchirurgischen Eingriffen werden zunehmend in der Fachliteratur dokumentiert, wobei die Infektion auf die Verwendung der Hypothermiegeräte während der extrakorporalen Zirkulation zurückzuführen ist [16,17]. Die durch die Studie gewonnenen Erkenntnisse sollen als Grundlageninformation für Forschungsarbeiten dienen, die sich mit der Fragestellung der alternativen Oxygenator-Entwicklung ohne den Einsatz eines Hypothermiegerätes beschäftigen. Die vorliegende Studie zeigt erstmals, dass die Regulation der Bluttemperatur mit Hilfe von Gas möglich ist und liefert einen Beitrag zum entsprechenden Forschungsgebiet.
Limitationen
Einen zentralen Limitationsaspekt der Studie stellt die Verwendung von Wasser als alternatives Testmedium anstelle von Blut dar. Abweichungen in Bezug auf die errechneten Leistungsfaktoren können aufgrund der geringfügig unterschiedlichen Wärmeleitfähigkeiten der beiden Medien entstehen.
Schlussfolgerung
Die Wärmeübertragung an der Hohlfasermembran konnte in der vorliegenden experimentellen Studie spezifiziert und über errechnete Leistungsfaktoren quantifiziert werden. Eine Gastemperatur-abhängige Wärmeübertragung an der Hohlfasermembran ist maßgeblich von dem Verhältnis zwischen der Gastemperatur am Oxygenator-Eingang und der Bluttemperatur abhängig. Zu Leistungsfaktoren in Bezug auf die FiO2-Konzentration können keine Rückschlüsse auf die Wärmeübertragung an der Hohlfasermembran gezogen werden. Hinsichtlich der Blutflussrate zeigen die Ergebnisse, dass niedrige Blutflusseinstellungen in Kombination mit einem hohen Gasfluss die Wärmeübertragung an der blutumströmten Kapillare begünstigt. In Bezug auf die getesteten Oxygenator-Modelle werden bei dem Modell von Inspire 7M, Sorin höhere Leistungsfaktoren im Rahmen der Wärmeübertragung erzielt als bei den Vergleichsoxygenatoren. Daraus kann geschlossen werden, dass sich eine kontrollierte Strömungsführung im Inneren des Oxygenators positiv auf die Wärmeübertragung entlang der Hohlfasermembran auswirkt.
Interessenskonflikt
Die Autoren haben keine finanziellen Interessen oder Beziehungen, die zu Interessenkonflikten führen können.
Ethik
Es wurden keine Versuche an Menschen und Tieren durchgeführt.
Wissenschaftlicher Kurzlebenslauf
Amalia Saunders studierte Molekulare und Technische Medizin (B.Sc.) an der Hochschule Furtwangen (Campus Schwenningen) und absolvierte im Anschluss den Masterstudiengang Technical Physician (M.Sc.). Seit November 2024 ist sie in der Thorax-, Herz- und Gefäßchirurgie des Universitätsklinikums Tübingen als Perfusionistin und weiterhin als stellvertretende Sprecherin des Jungen Forums der Deutschen Gesellschaft für Perfusiologie und Technische Medizin tätig.